微侵入脑深部神经调控是神经科学与神经工程领域长期关注的脑机接口关键技术问题,对脑功能解析和神经疾病干预具有重要意义。低强度聚焦超声(LIFU)因其优良的组织穿透能力和空间聚焦特性,被认为是实现深部、无线神经调控的潜在重要技术手段。然而,单独依赖超声本身的神经调控效应会导致调控效果过度依赖神经元亚型、力敏离子通道表达及局部组织力学环境,进而导致刺激响应呈现异质性,限制了最终调控效果的稳定性、可预测性和可控性。近年来,引入功能化纳米颗粒作为“声-电/声-力”能量转换单元,被认为是极具前景的提升超声神经调控可控性和一致性的策略。因此,发展无需转基因、无需电极植入、可在低强度超声条件下实现稳定、可预测神经激活的纳米尺度能量转换与调控技术方法,对推动无线神经调控技术的精细化和临床转化具有重要意义。
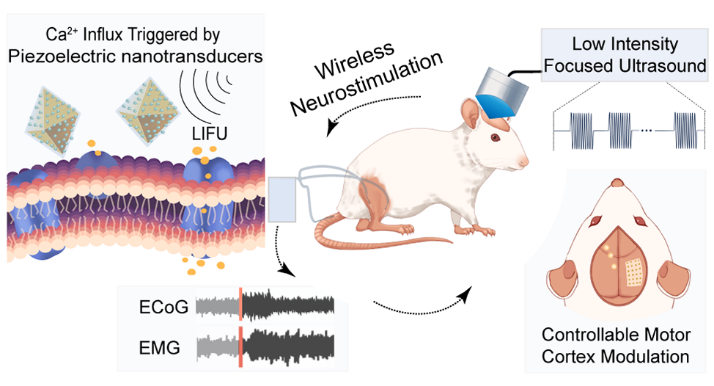
图1. 聚集增强压电纳米换能器介导的无线超声神经调控示意图
近日,清华大学生物医学工程学院张明君团队与首都医科大学三博脑科医院闫长祥团队研究了一种基于功能化纳米颗粒的聚集增强压电纳米换能方法,用于在低强度聚焦超声下实现无线神经刺激。该研究以“Aggregation-Enhanced Piezoelectric Nanotransducers Facilitate Transgene-Free Wireless Neurostimulation under Low-Intensity Focused Ultrasound”为题发表在 《ACS Nano 》期刊上。低强度超声本身具有良好的组织穿透性和空间聚焦能力,被视为深部神经调控的重要技术手段,但其神经调控效果往往受组织与细胞差异影响而存在不确定性。该研究通过将 10 nm 钛酸钡(BaTiO₃)压电纳米颗粒组装至多孔 UiO-66 金属有机框架表面,并引入导电聚多巴胺包覆,构建亚微米级 pDA-BTO/UiO-66 纳米复合结构,从而显著增强超声驱动下的局域电场转换效率并提升神经响应的一致性,同时有效降低细胞内吞。实验结果表明,该纳米换能体系可在分化 PC12 细胞中稳定诱发由电压门控离子通道介导的钙离子内流,并在大鼠运动皮层实现空间特异性的脑电响应及对应身体部位的肌电输出,其诱导的 c-Fos 表达水平与有创电极刺激相当。进一步的组织学分析显示,该纳米颗粒体系具备良好的神经安全性和生物相容性。该工作表明,纳米颗粒辅助的超声能量转换是一种极具前景的无线神经调控路径,为低强度超声驱动的稳定、可控神经刺激及微纳换能器设计提供了重要参考。
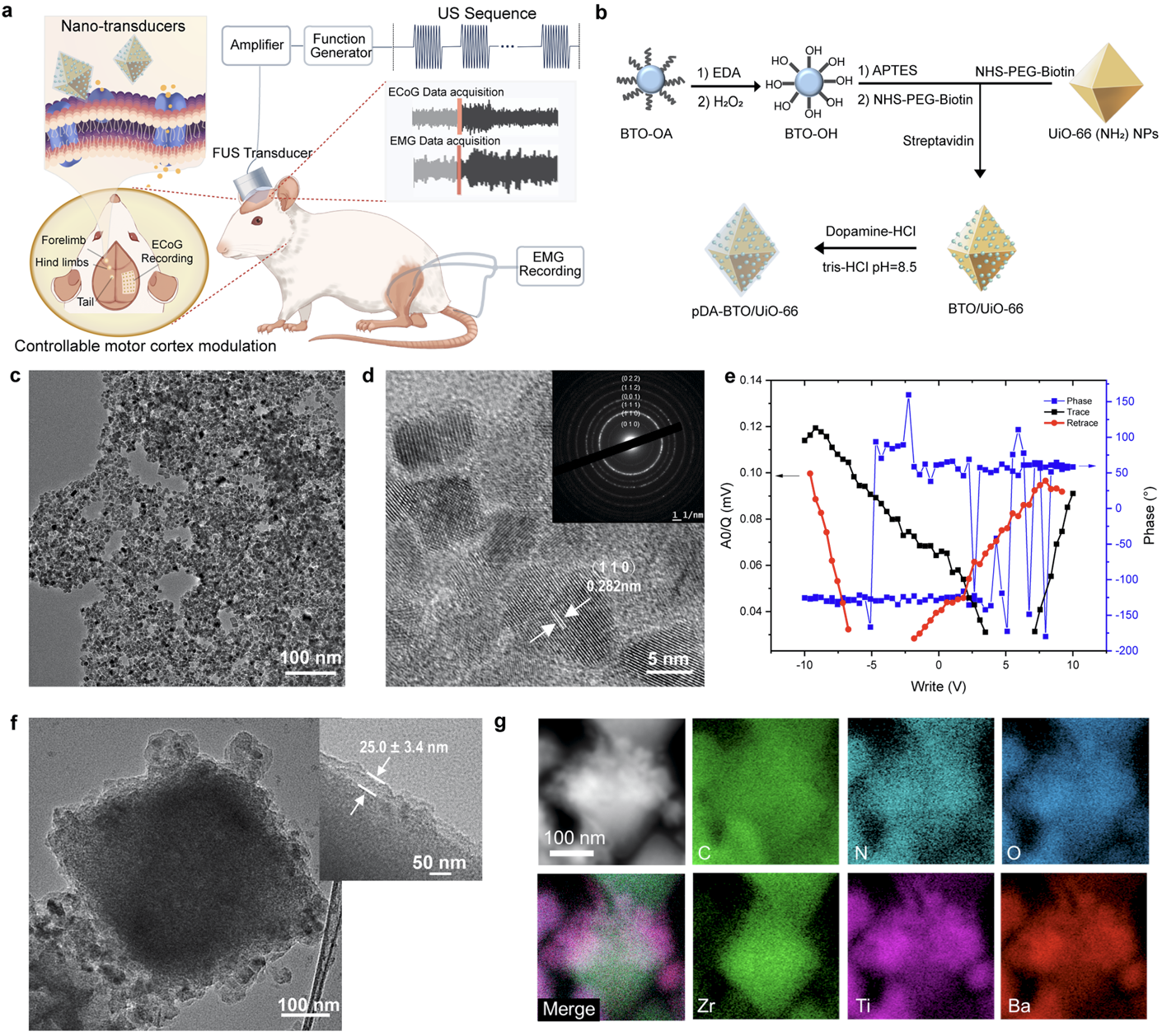
图2. 通过压电纳米换能器实现无线神经调控的研究思路示意图和材料表征
为解决分散的单个压电纳米粒子产生的局部电场微弱,且易被细胞吞噬,难以有效地刺激神经元的问题,本研究提出“聚集增强”压电纳米换能器的设计思想。该设计以 UiO-66 金属有机框架作为核心,为压电组分提供高表面积比的负载平台和丰富的表面活性位点;在其表面密集组装 10 nm钛酸钡压电纳米颗粒,使其在超声驱动下产生协同压电效应,进一步增强局部电场输出;外层引入导电聚多巴胺(pDA)涂层,提升材料的生物相容性和胶体稳定性,并进一步优化局域电场的耦合与传递,达到提高导电特性的目的。该结构设计使纳米换能器能在低强度超声条件下产生提升压电输出,并更倾向于附着于细胞膜表面,从而实现持续、有效的膜相关电刺激(图3)。
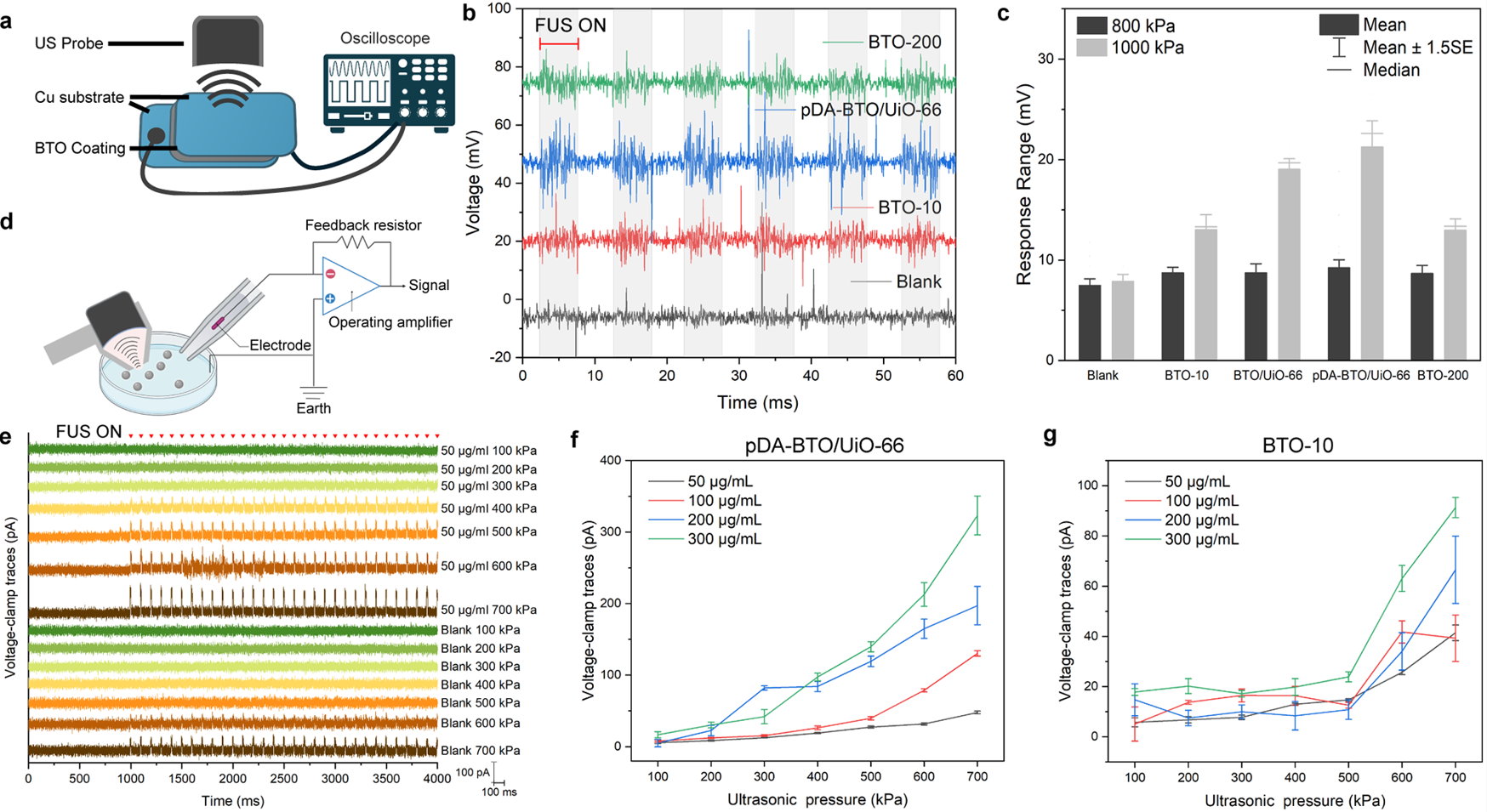
图3. 压电纳米换能器在LIFU下的响应测试
在 PC12 神经元样细胞模型中(图4),该超声驱动的压电纳米换能器能够以可调方式诱发细胞内钙离子内流,表明其具备有效的神经激活能力。进一步的机制研究显示,该钙响应主要依赖于细胞外钙离子的内流过程,并可被电压门控钠离子通道或钙离子通道抑制剂显著阻断,而机械敏感通道抑制对其影响有限。这些结果表明,该设计可以通过压电效应诱导膜电位变化,激活电压门控离子通道进一步实现神经调控,而非依赖机械刺激机制。
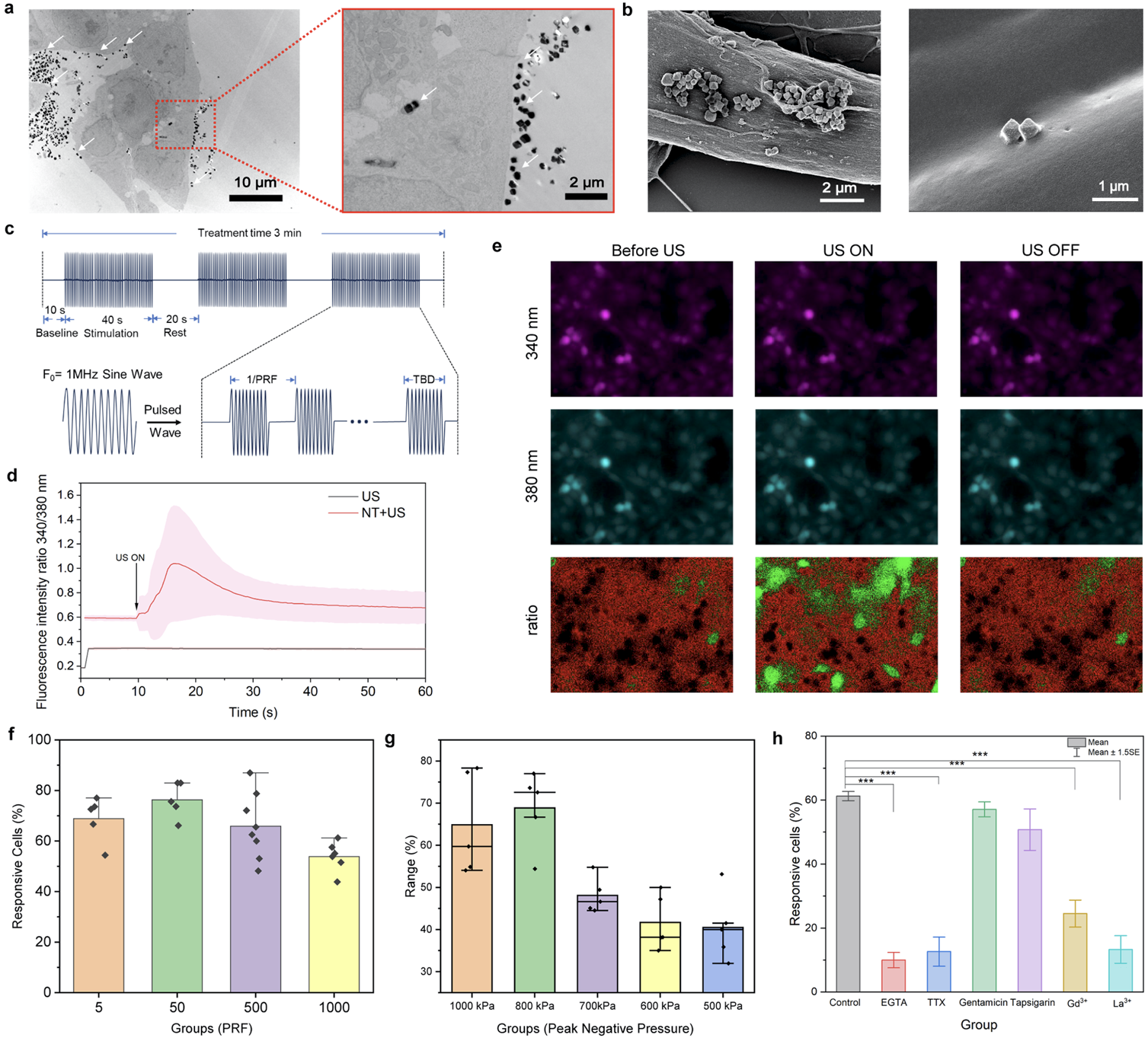
图4. 纳米换能器介导的体外压电神经刺激和机理研究
将上述压电纳米换能器注射至大鼠运动皮层特定区域后施加低强度聚焦超声刺激(图5),可在皮层脑电(ECoG)记录中观察到强烈且稳定的神经响应。同时,肌电图(EMG)结果显示,刺激不同功能亚区的运动皮层(分别对应前肢、后肢和尾部),能够诱发相应身体部位特异性的肌肉活动,表明该体系具备良好的空间选择性和功能特异性。进一步的 c-Fos 免疫荧光染色分析证实,刺激区域神经元被显著激活,其激活水平与有创电极刺激产生的效果相当,验证了该无线神经调控策略在在体条件下的有效性。
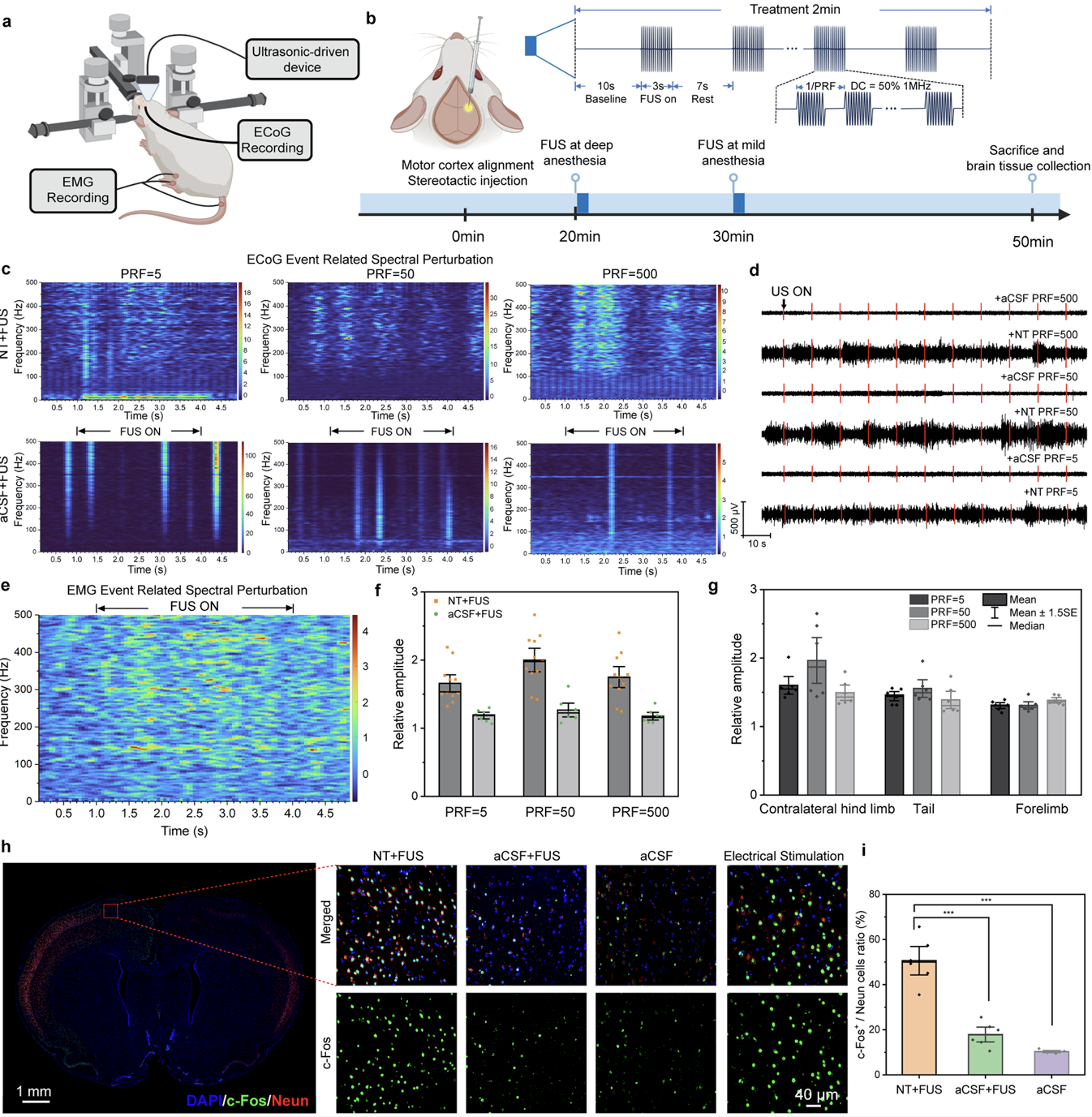
图5. 纳米换能器对大鼠运动皮层的多位点压电神经刺激。
生物安全性评估结果(图6)表明,该纳米换能系统在脑组织中可以被快速清除,短期和长期的组织学评估显示,该处理未引起神经元损失,也未增加星形胶质细胞或小胶质细胞密度,表明其具有良好的生物相容性和神经安全性。
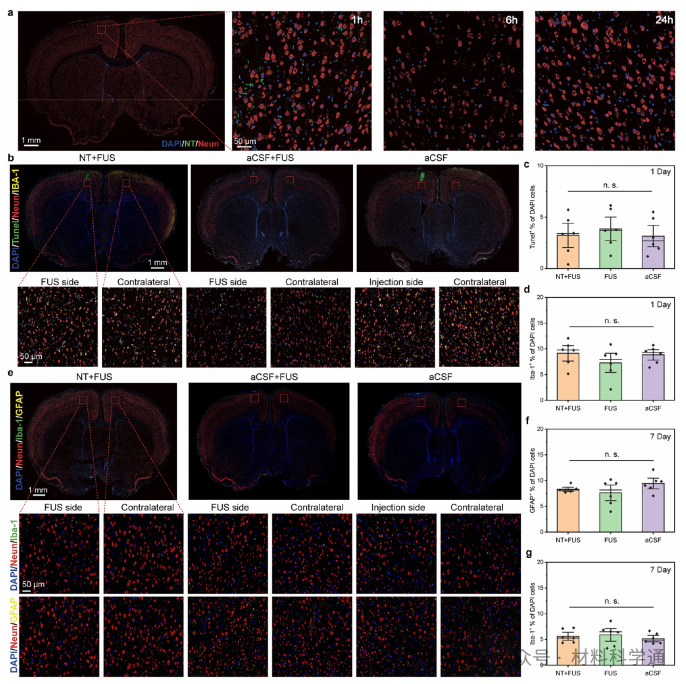
图6. 生物安全性评估
本研究提出了一种无需转基因、无需电极植入的无线神经调控范式,其中低强度超声作为具有脑深部穿透能力的能量载体,而功能化压电纳米颗粒则作为核心且高度前瞻性的能量转换与调控单元。通过微纳材料结构设计,超声能量被转化为局域电刺激,从而实现对神经活动的稳定、可预测调控,并在机制上显著弱化了对力敏离子通道异质性的依赖。展望未来,结合血脑屏障可逆开放等非侵入式递送策略,该微纳米颗粒辅助的超声神经调控体系有望在基础神经科学研究和潜在临床神经调控应用中展现更多的发展空间。
清华大学生物医学工程学院张明君教授和首都医科大学三博脑科医院闫长祥教授为共同通讯作者;清华大学生物医学工程学院2023级博士研究生崔承前,清华大学生物医学工程学院博士后(2025届博士毕业生)高喜泽为共同第一作者。清华大学生物医学工程学院2022级博士研究生杜念臻,2024级博士研究生李经纬,对本研究有重要贡献。
原文链接:
https://doi.org/10.1021/acsnano.5c15915