细胞外囊泡(Extracellular Vesicles, EVs)是细胞释放的纳米级囊泡,广泛存在于血液、尿液、脑脊液等多种体液中。它们携带着来源细胞的RNA、DNA和蛋白信息,是反映疾病状态的重要“分子信使”。然而,传统EV分析通常依赖超速离心或多步纯化流程,不仅耗时、操作复杂,还容易造成样本损耗,限制了临床和大规模应用。
近日,清华大学生物医学工程学院胡晔教授团队联合美国杜兰大学宁波教授研究了一种用于液体活检的创新检测方法:脂质体–细胞外囊泡融合(Liposome–EV Fusion)+ CRISPR 分子诊断体系。该方法通过将核酸扩增与CRISPR检测系统直接递送进入EV内部,实现对体液中低丰度分子标志物的高灵敏、免分离检测,为感染性疾病、肿瘤及神经系统疾病的早期诊断提供了新的技术路径。相关研究成果以《液体活检中检测试剂直接递送至细胞外囊泡用于生物标志物分析》(Direct delivery of assay reagents to extracellular vesicles in liquid biopsies for biomarker analysis)为题,于2026年1月30日发表在《Nature Protocols》期刊上。

点击查看更多论文信息
创新方法亮点
该研究分为四个关键阶段:脂质体构建 、EV抗体捕获 、脂质体–EV融合 、 CRISPR信号输出,具体解决方案如下:
把检测系统“送进”细胞外囊泡:利用工程化脂质体包裹核酸扩增和CRISPR检测试剂,在融合后进入EV内部进行原位反应
免去复杂分离步骤:通过抗体捕获EV并直接检测,减少样本处理带来的误差和损耗
高度灵敏与通用性强:只需更换引物和gRNA,就能从病毒RNA检测拓展到肿瘤miRNA、突变DNA等多类标志物检测
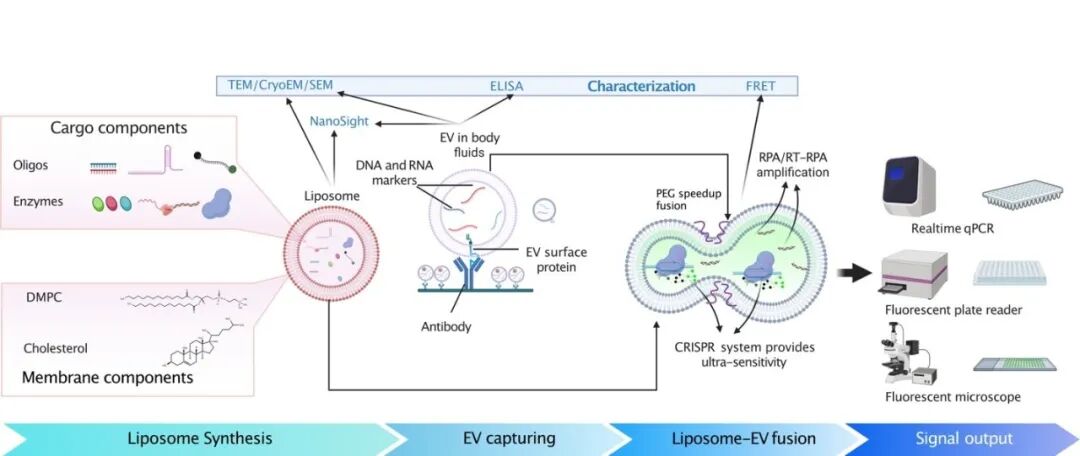
整体工作流程示意图
方法流程解读
捕获EV:在检测板表面固定抗体,选择性“抓住”样本中的EV
融合递送:加入装载检测体系的脂质体和促进融合的PEG,使脂质体与EV膜融合
信号放大:EV内部发生等温扩增和CRISPR识别反应,产生可检测的荧光信号
读出结果:通过酶标仪、实时PCR或荧光成像系统完成定量分析
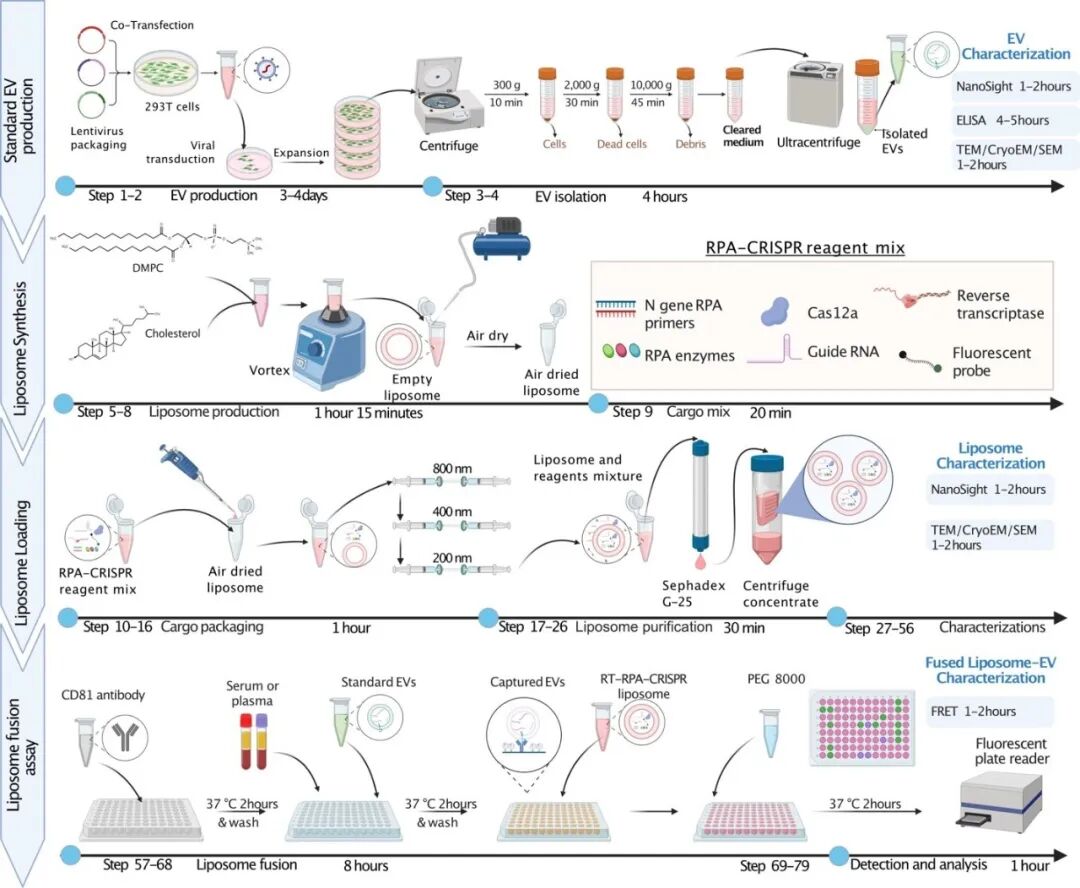
方法步骤图解
应用前景
医学诊断:病毒感染、肿瘤标志物、治疗响应监测
基础研究:EV异质性、细胞间通讯机制解析
转化医学:便携式检测平台与临床标准化流程建设
工程与材料学:脂质体与生物膜融合机制研究
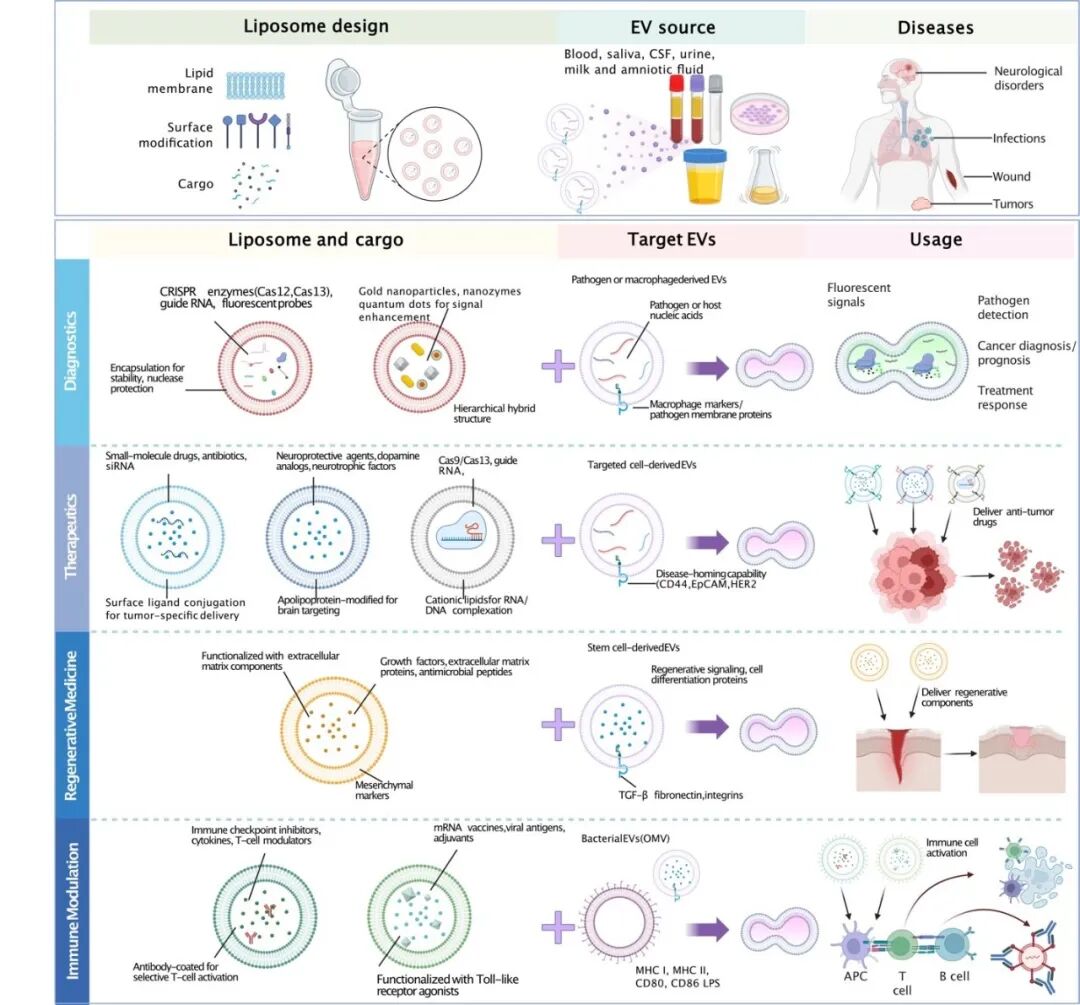
多学科应用场景示例
该成果体现了胡晔教授团队在生物医学工程、分子诊断与纳米技术交叉领域的持续创新能力,也为构建“从基础研究到临床转化”的技术平台提供了示范路径。该体系兼具标准化潜力与工程可扩展性,对推动科研成果服务公共健康与精准医疗具有重要意义。