自新冠疫情暴发以来,SARS-CoV-2(严重急性呼吸综合征冠状病毒2型)持续对全球公共卫生造成深远影响。除感染带来的住院和死亡风险外,SARS-CoV-2还可能导致长期症状、反复感染及持续性的健康负担。与此同时,细颗粒物PM2.5(直径≤2.5微米的颗粒物)作为全球最重要的环境健康风险因素之一,广泛来源于燃料燃烧、交通排放、工业活动及复杂的大气化学过程,可对呼吸系统、心血管系统和神经系统造成多维度危害。近年来,越来越多流行病学研究提示,PM2.5暴露可能与COVID-19(2019冠状病毒病)相关的不良结局有关,包括感染、住院和死亡风险升高。已有研究还表明,PM2.5不仅可能损伤呼吸系统、诱导免疫和炎症反应,还可能作为载体增加病毒负载,甚至促进病毒进入和复制。然而,尽管PM2.5与SARS-CoV-2风险升高相关这一现象已在群体层面得到关注,其背后的分子机制仍缺乏系统性解释:PM2.5究竟通过哪些细胞通路、关键基因和基因-环境互作,影响宿主对病毒的易感性,仍是一个悬而未决的问题。
2026年3月30日,清华大学生物医学工程学院2021级博士生冯国庆以第一作者身份在Nature系列期刊《自然·通讯》(Nature Communications)上发表了题为“人工智能辅助的多组学分析揭示PM2.5暴露下NPC1介导的SARS-CoV-2易感性”( AI-guided multi-omics analysis identifies NPC1-modulated susceptibility to SARS-CoV-2 infection under PM2.5 exposure)的研究论文。

点击获取更多论文信息
研究概述
研究团队首先利用微调的单细胞转录组基础模型,识别出PM2.5暴露与SARS-CoV-2感染之间共享的转录组特征和通路信号;随后结合UK Biobank(英国生物样本库)人群数据开展流行病学分析,验证PM2.5暴露与SARS-CoV-2感染风险增加之间的正相关关系;进一步通过全基因组关联分析(GWAS)和功能基因组学分析,锁定了NPC1和RMC1附近的关键遗传位点,并重点识别出NPC1作为重要调控因子。体外实验进一步表明,携带病毒的PM2.5可增强感染过程,而抑制NPC1表达或敲除相关调控位点后,病毒感染能力明显下降。综合这些证据,研究提出:PM2.5可能作为病毒载体促进其经非受体依赖性的内吞方式进入细胞,并通过NPC1调控的内吞-溶酶体通路增强SARS-CoV-2的感染效率。
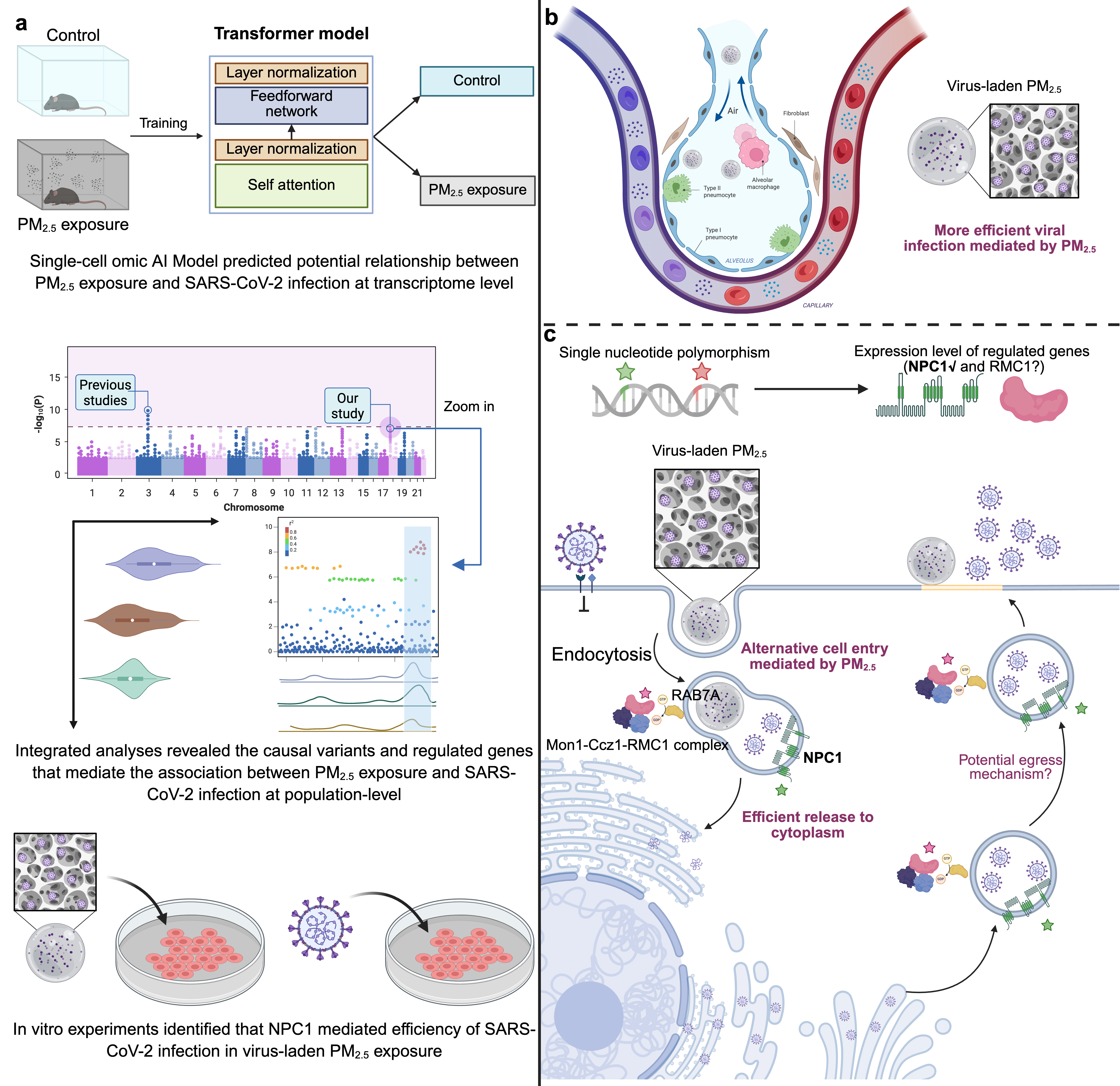 研究框架与机制示意图
研究框架与机制示意图
研究结果
1 单细胞转录组AI模型能够稳定识别PM2.5暴露状态
研究基于小鼠肺组织样本的单细胞转录组数据构建了PM2.5暴露分类模型。结果显示,经过预训练并微调的Geneformer模型在识别PM2.5暴露状态方面表现稳健,且在bulk RNA-seq外部数据以及未进入训练集的细胞类型的泛化测试中均优于从零训练的BERT模型。这表明预训练权重有助于模型捕捉跨细胞类型、跨数据模态共享的PM2.5分子响应模式。
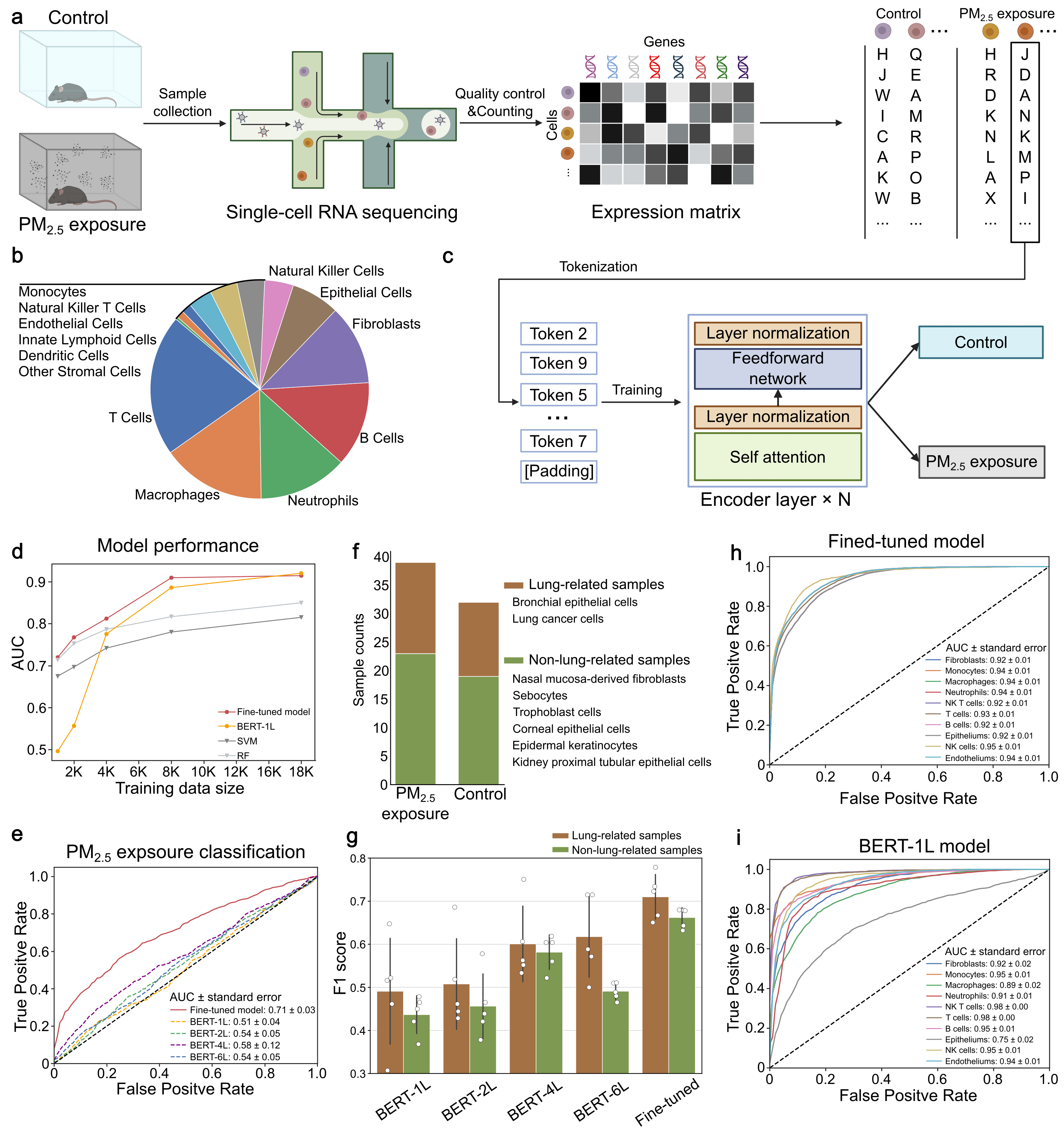
Figure1:PM2.5暴露的单细胞组学微调模型实现暴露状态分类
2 通路特征与人群证据共同支持PM2.5提高SARS-CoV-2感染风险
通过in silico基因扰动分析,研究发现PM2.5相关基因显著富集于COVID-19、核糖体、免疫应答以及吞噬体/溶酶体等囊泡运输相关通路,提示PM2.5暴露可能通过影响抗病毒反应和胞内运输过程增强病毒感染。进一步在英国生物银行中开展流行病学分析后,研究观察到个体年均和月均PM2.5暴露水平均与SARS-CoV-2感染呈显著正相关,且在不同滞后时间和亚组分析中结果一致。
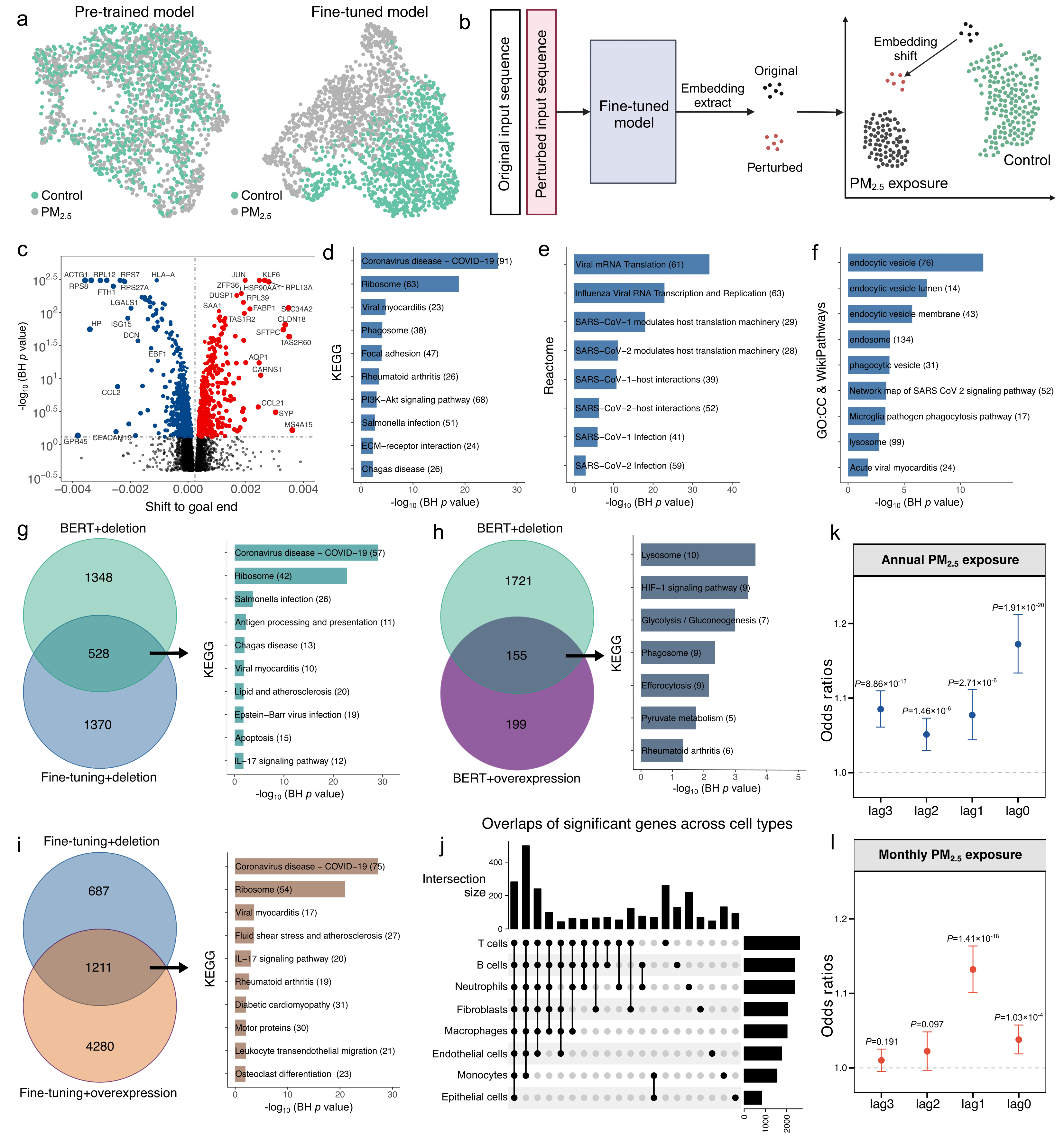
Figure2:扰动分析与流行病学分析揭示PM2.5暴露与COVID-19的潜在关联
3 GWAS鉴定出调节PM2.5与SARS-CoV-2感染关联的关键基因区域
在遗传层面,研究首先确认了3p21.31区域与COVID-19阳性结果相关的经典位点。随后针对基因-环境互作开展分析,发现18q11.2区域的一组SNP(单核苷酸多态性)簇显著富集,定位于NPC1与RMC1附近。结果提示,在较高PM2.5暴露背景下,携带风险等位基因的个体更易发生SARS-CoV-2感染,表明该区域可能是环境暴露影响SARS-CoV-2易感性的遗传调节位点。
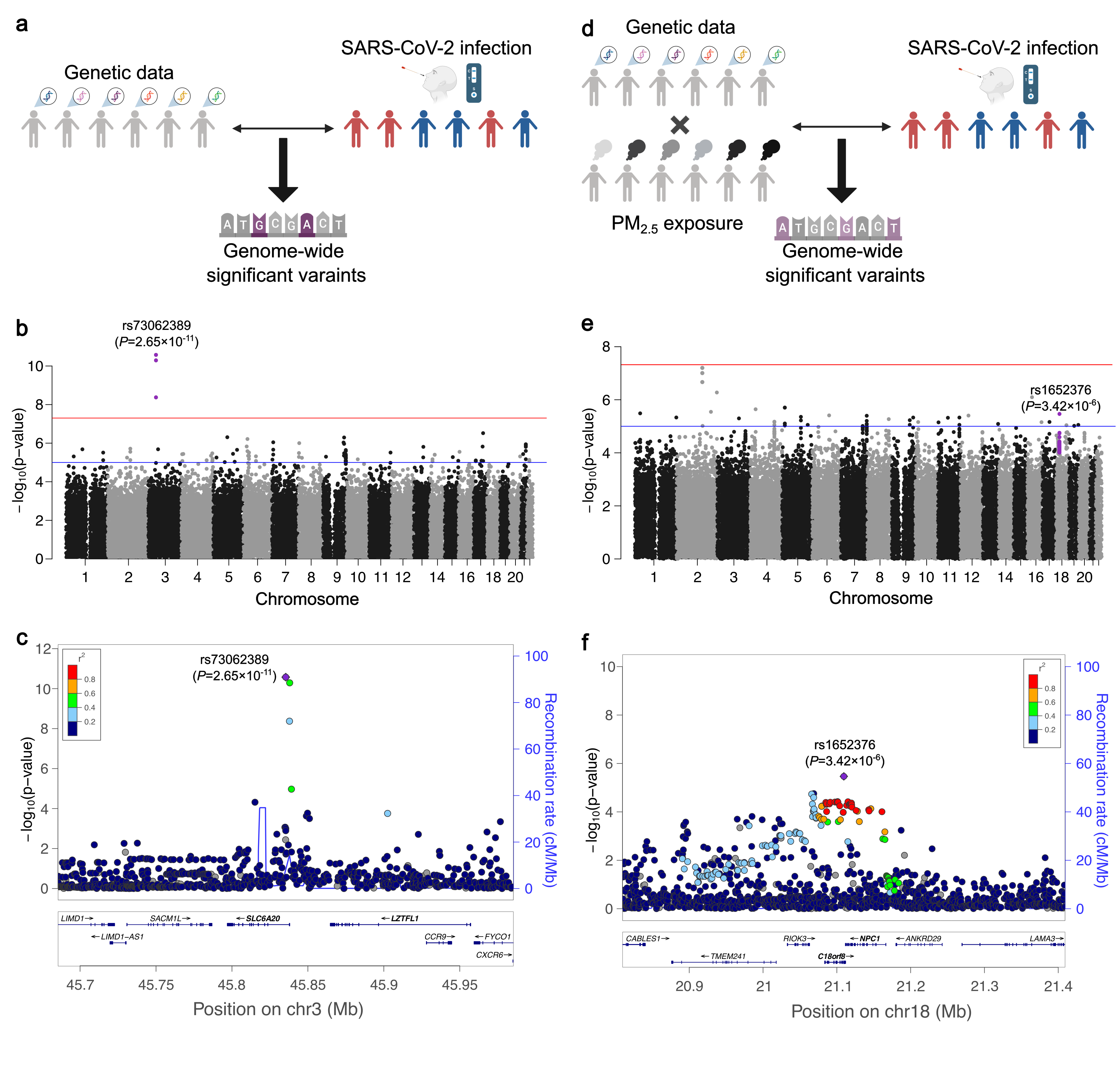
Figure3:GWAS鉴定PM2.5与SARS-CoV-2感染相关的基因组位点
4 候选因果基因组变异及肺组织特异性调控机制指向NPC1/RMC1通路
对与lead SNP强连锁不平衡的变异进行功能注释后,研究锁定了4个位于开放染色质区域的候选变异,其中rs1788783在肺相关细胞中显示出最强的调控信号。eQTL分析显示,这些风险等位基因与肺组织中NPC1和RMC1表达升高相关;孟德尔随机化进一步支持这两个基因表达升高会增加SARS-CoV-2易感性。结合单细胞表达谱和in silico基因扰动结果,研究提示NPC1/RMC1可能通过内吞、溶酶体和自噬相关过程协同调控SARS-CoV-2感染。
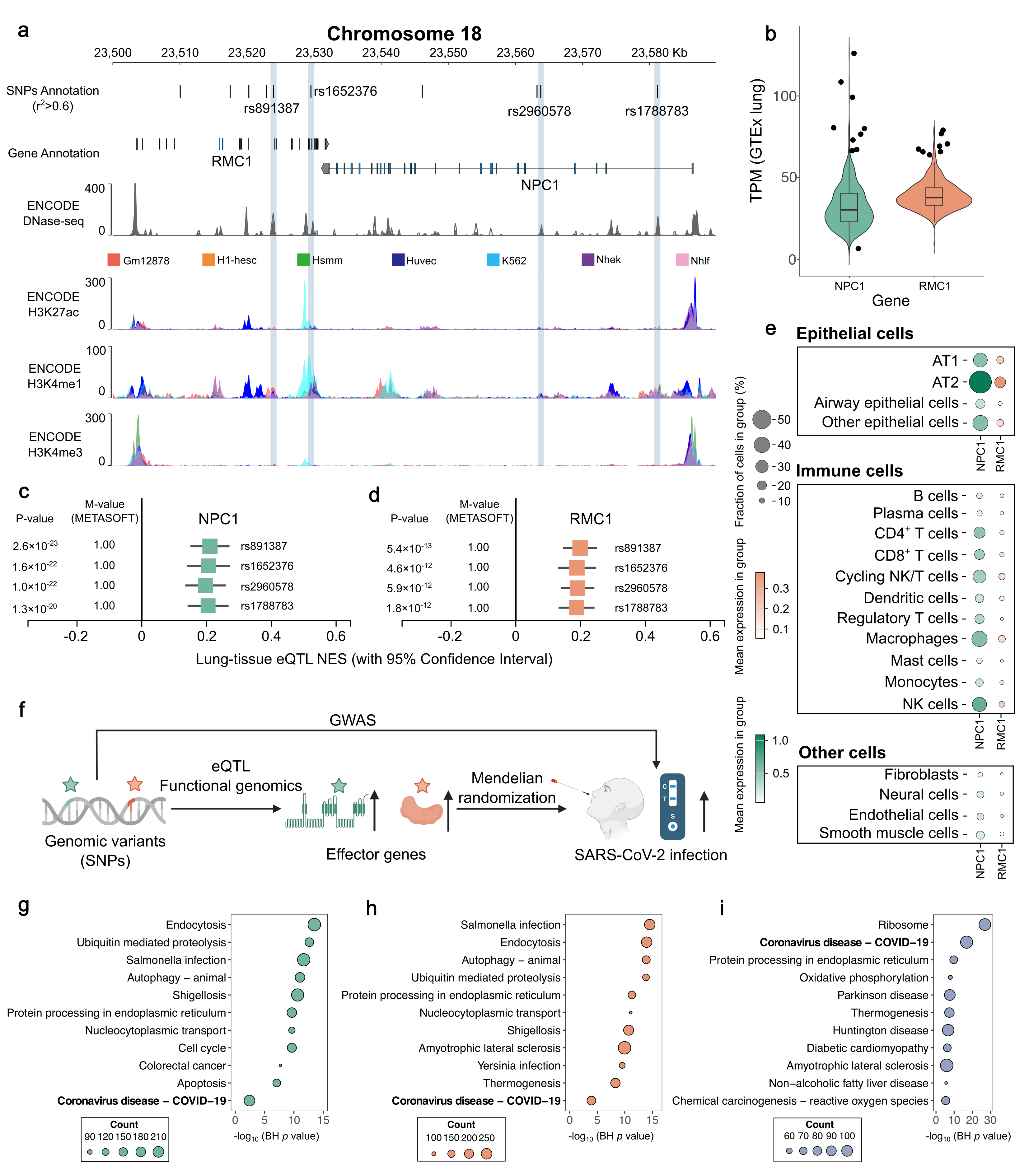
Figure4:NPC1与RMC1在PM2.5暴露与SARS-CoV-2感染关联性中的潜在调控作用
5 体外实验验证rs1788783-NPC1轴在“PM2.5负载病毒”的暴露条件下调控感染
在A549细胞中,CRISPR敲除候选位点后发现,靶向缺失rs1788783所在区域可显著降低NPC1蛋白表达,而对RMC1影响不明显。进一步构建游离病毒与PM2.5负载病毒两种暴露情境后,研究发现后者可增强SARS-CoV-2假病毒感染能力;而这种强化的感染能力在rs1788783敲除细胞中被显著抑制。使用siRNA下调NPC1后也观察到一致结果,说明NPC1是促进SARS-CoV-2在PM2.5暴露场景下高效感染的重要效应分子。
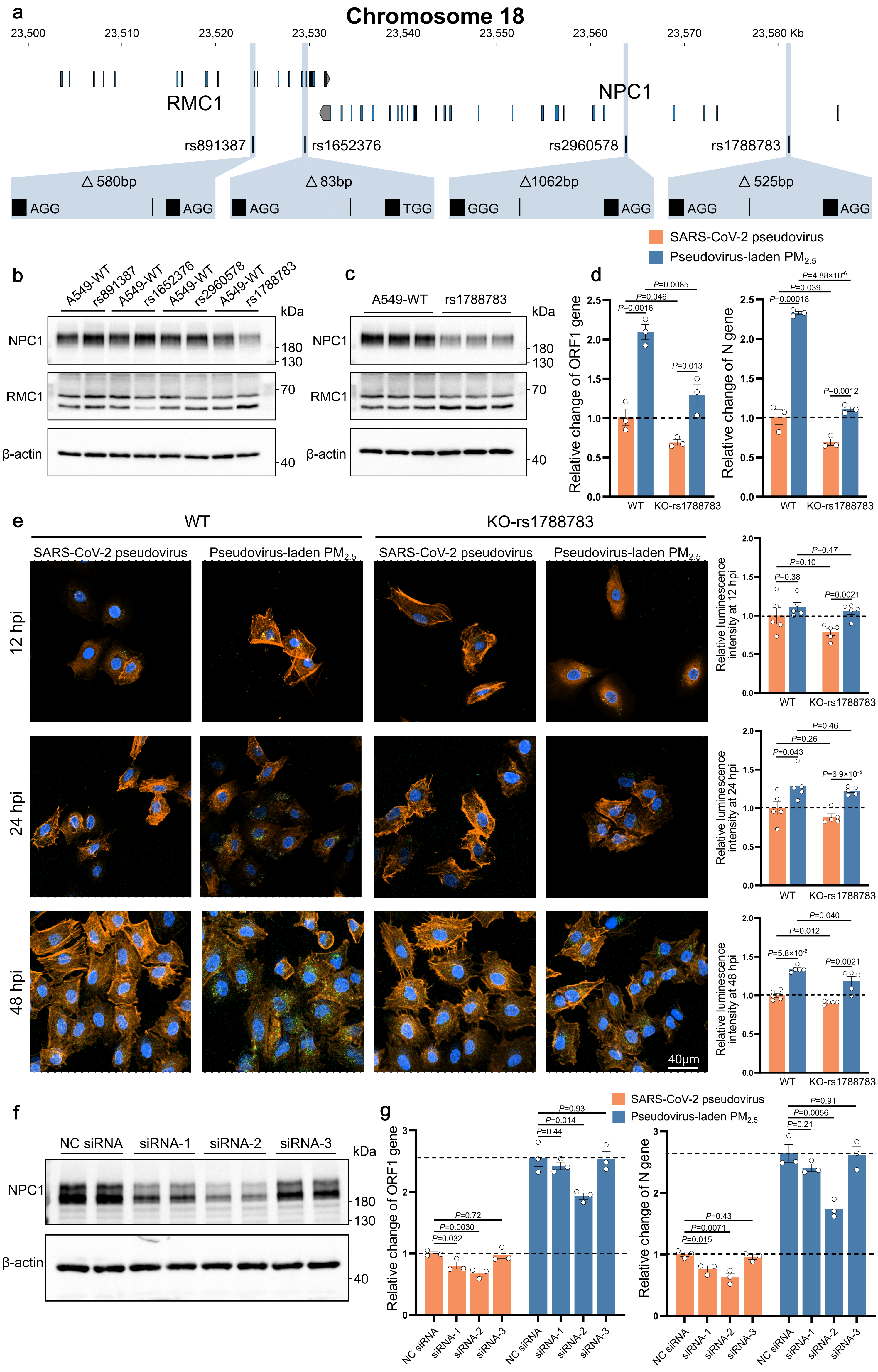
Figure5:负载病毒的PM2.5暴露增强SARS-CoV-2感染并受到NPC1调控
研究结论
本研究通过人工智能、多组学分析与实验验证相结合,系统揭示了PM2.5暴露通过NPC1相关的内吞-溶酶体通路增强宿主对SARS-CoV-2的易感性。本研究不仅为理解空气污染与病毒感染之间的生物学联系提供了新机制,也为识别环境暴露背景下的高风险人群和潜在干预靶点提供了新线索。
清华大学生物医学工程学院2021级博士研究生冯国庆为论文第一作者,清华大学万科公共卫生与健康学院底骞副教授、山东第一医科大学(山东省医学科学院)医学科技创新中心董政副教授为论文共同通讯作者。
原文链接:https://www.nature.com/articles/s41467-026-71196-3