研究背景
肝脏是人体的核心代谢器官,其功能异常与全球三分之一人口的疾病相关。磁共振成像(MRI)可提供高分辨率的解剖与功能信息,但常规动态增强MRI需注射钆对比剂,存在过敏、肾源性系统性纤维化及钆沉积风险,且不适用于肾功能不全患者。
化学交换饱和转移(CEST)MRI能够通过检测内源性代谢物(如蛋白质/多肽、糖原、葡萄糖、肌酸等)实现无标记代谢成像。然而,腹部CEST面临两大瓶颈:扫描时间过长(>5分钟)和呼吸运动敏感(成功率仅60%-70%),导致其长期无法进入临床常规应用。
肝脏肿瘤诊断长期依赖外源性对比剂注射,不仅增加患者负担与肾毒性风险,更不适合需要多次复查的肿瘤随访。针对免标记代谢磁共振长期以来"看不清、扫不动"的临床痛点——微弱代谢信号导致扫描慢,呼吸运动导致图像模糊——清华大学生物医学工程学院宋小磊团队研发了空间-频谱协同编解码(Spatial-Spectral Encoding, SSE)的超快CEST-MRI技术。SSE-CEST以超40倍加速实现了单次屏气、全肝覆盖、无外源性标记的3D高清代谢成像。该技术在糖原仿体、离体猪肝、健康志愿者及肝癌患者中完成了系统验证,能够同时探测酰胺、糖原、脂肪族NOE及葡萄糖代谢。SSE-CEST实现了肝肿瘤病人微小复发灶的精准识别和定位,与 PET 及钆对比剂诊断高度吻合,标志着免标记代谢磁共振从科研向临床诊疗的关键跨越。相关研究成果于2026年3月31日发表于Nature Communications。

点击查看更多论文信息
研究方法
本研究提出了一种空间-频谱编码(SSE)CEST-MRI方法(图1),核心创新包括:
1、超快z-ω编码采集:在饱和脉冲期间沿选层方向施加梯度(Gsat),使不同空间位置的质子同时被不同频率饱和,一次采集即获得一条对角线状的z-ω采样线。通过多条平行、放射或钻石形轨迹,在10-11次采集内完成对全频谱的高效覆盖。
2、数据驱动频谱重建:利用CEST谱的低秩特性,将相邻3层体素的稀疏采样数据合并,通过奇异值分解(SVD)提取频谱基函数,进而插值得到121个频率偏移的高密度谱(加速倍数44倍)。
3、单次屏气采集:结合并行成像与Dixon型3D-TFE读出,在18-21秒内完成全肝41层、多频偏移的3D图像采集,彻底消除呼吸运动伪影。
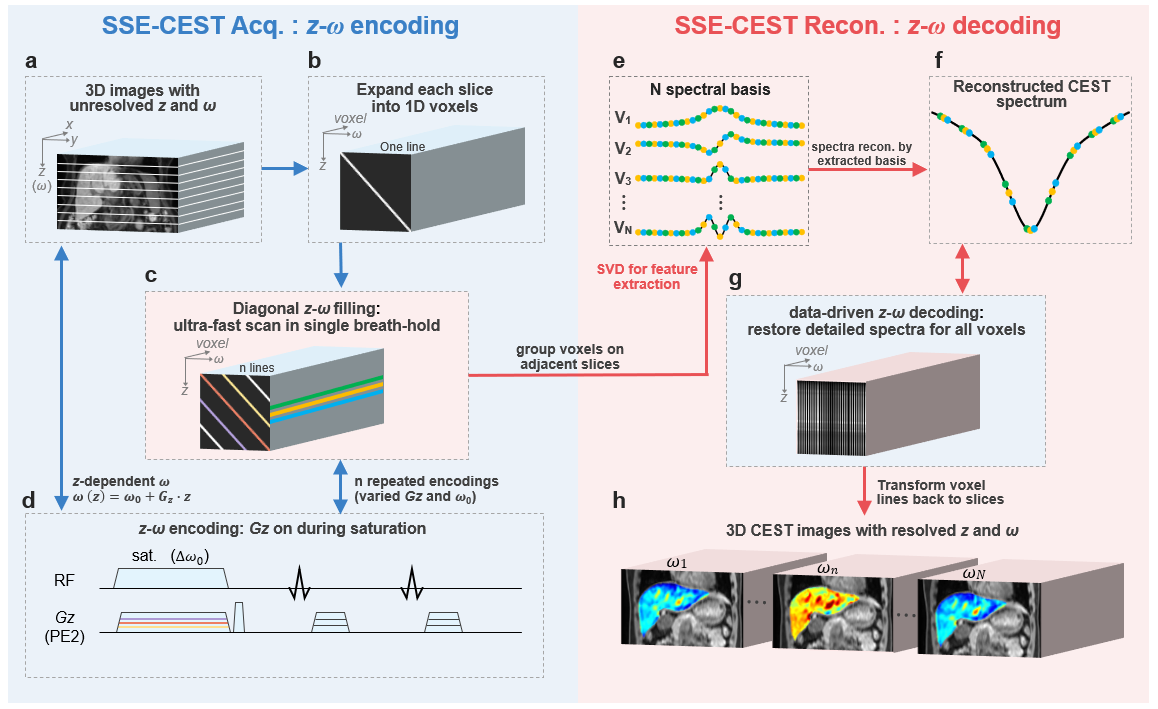
图1 基于空间-频谱编码(SSE)CEST-MRI的单次屏气代谢磁共振成像框架
实验设计
1、糖原仿体与离体猪肝验证:对比SSE-CEST与传统CEST,评估不同z-ω采样轨迹(平行、钻石、放射)的保真度。
2、健康志愿者:10名志愿者完成重复扫描验证可重复性;5名志愿者进行过夜空腹实验(餐后2小时 vs. 禁食12小时),评估多代谢物变化;另5名志愿者进行口服葡萄糖耐量试验(OGTT),动态监测葡萄糖代谢。
3、肝癌患者:纳入12例肝细胞癌(HCC)患者,包括活性病灶(n=11)与治疗后坏死灶(n=12),并与FDG-PET/CT及常规增强MRI对比。
实验结果
1、高保真度与可重复性
在糖原仿体中,SSE-CEST与传统CEST的糖原NOE信号高度相关(r=0.97,p<0.0001),且信号强度与糖原浓度呈线性相关(r=0.95,p<0.01)(图2)。健康志愿者重复扫描显示,24/40个对比图相关系数>0.99,ST@1.2 ppm与ST@3.5 ppm的两次扫描相关性分别为0.95和0.96(图3)。
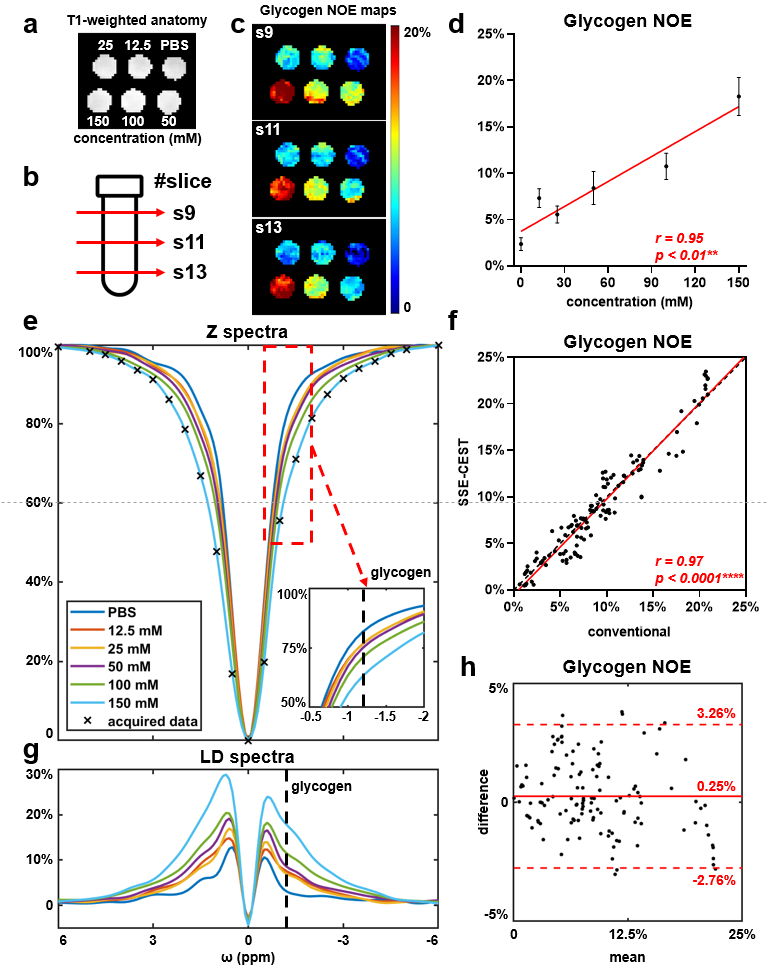
图2 使用1%琼脂的糖原仿体对SSE-CEST进行定量评估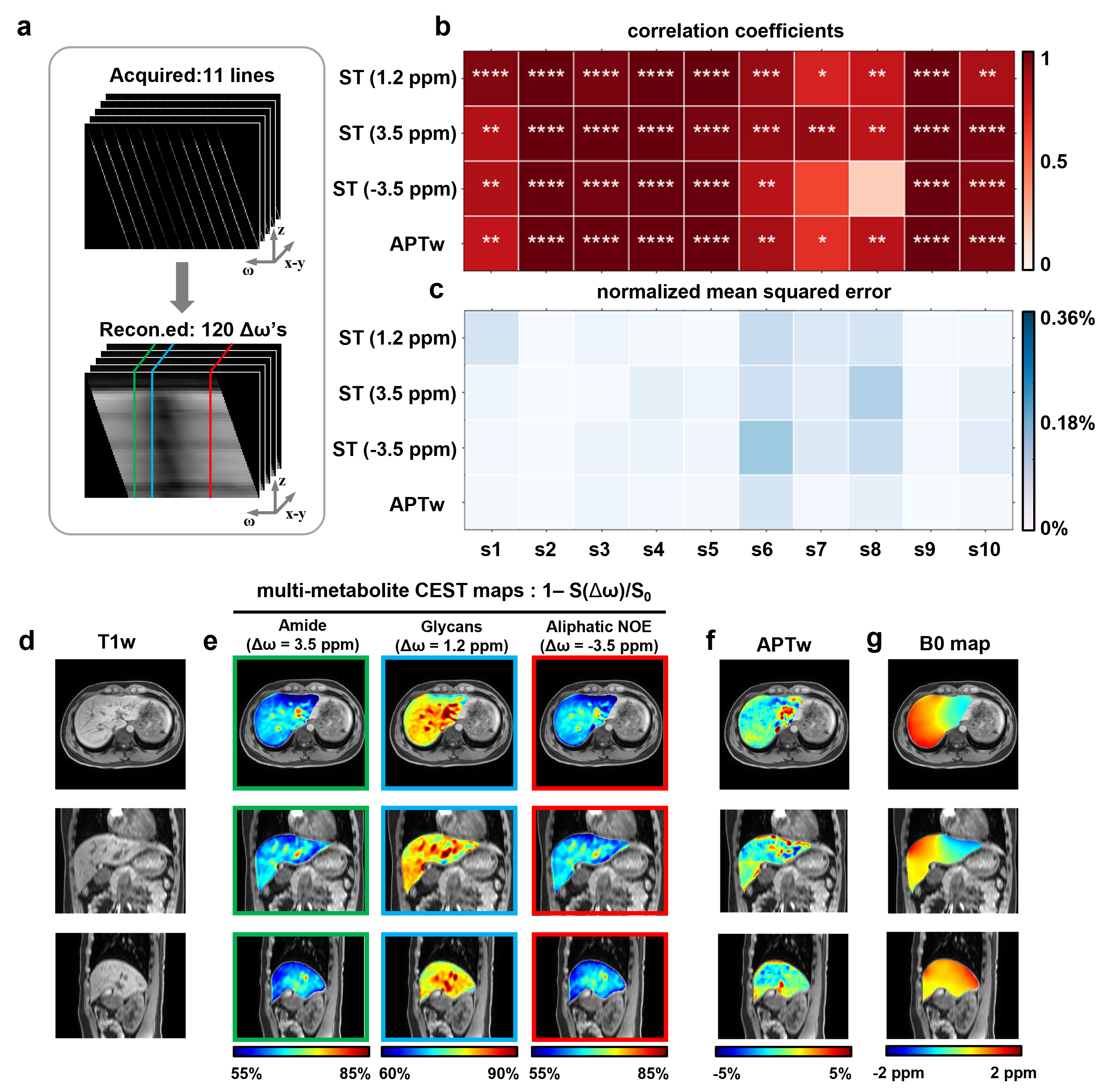

图3 健康志愿者SSE-CEST代谢成像
2、禁食实验
单次屏气SSE-CEST可同时获得酰胺CEST(3.5 ppm)、糖原NOE(-1.2 ppm)、脂肪族NOE(-3.5 ppm)、APTw及羟基CEST(1.2 ppm)等多种对比。在空腹实验中,禁食12小时后肝脏酰胺CEST、糖原NOE、脂肪族NOE、APTw及羟基CEST均显著下降(p值均<0.01),频谱变化清晰可辨。
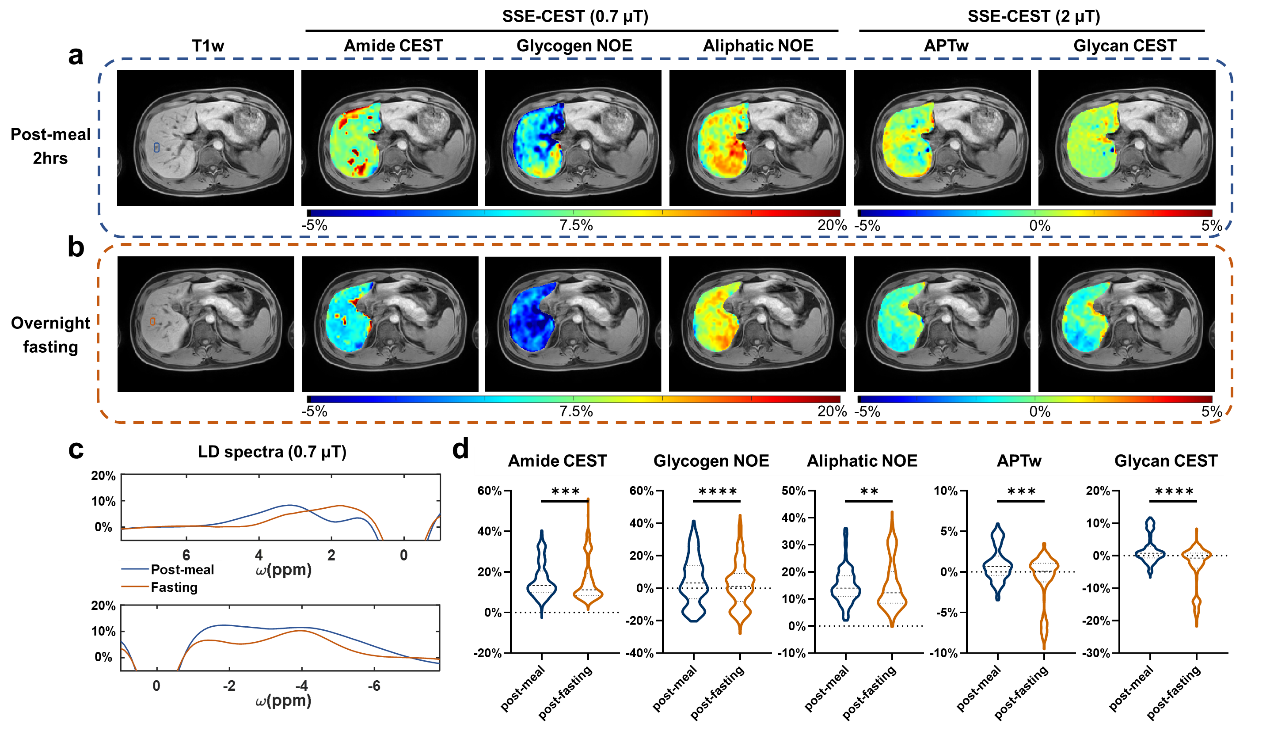
图4 SSE-CEST 技术用于评估禁食实验期间肝脏的代谢变化
3、口服葡萄糖动态代谢成像
在OGTT实验中,SSE-CEST连续监测至服葡萄糖后51分钟,肝脏MTRasym(2.1 ppm)信号在30分钟左右达到平台期,而T2变化不显著,证明了SSE-CEST对葡萄糖代谢的特异性检测能力(图5)。
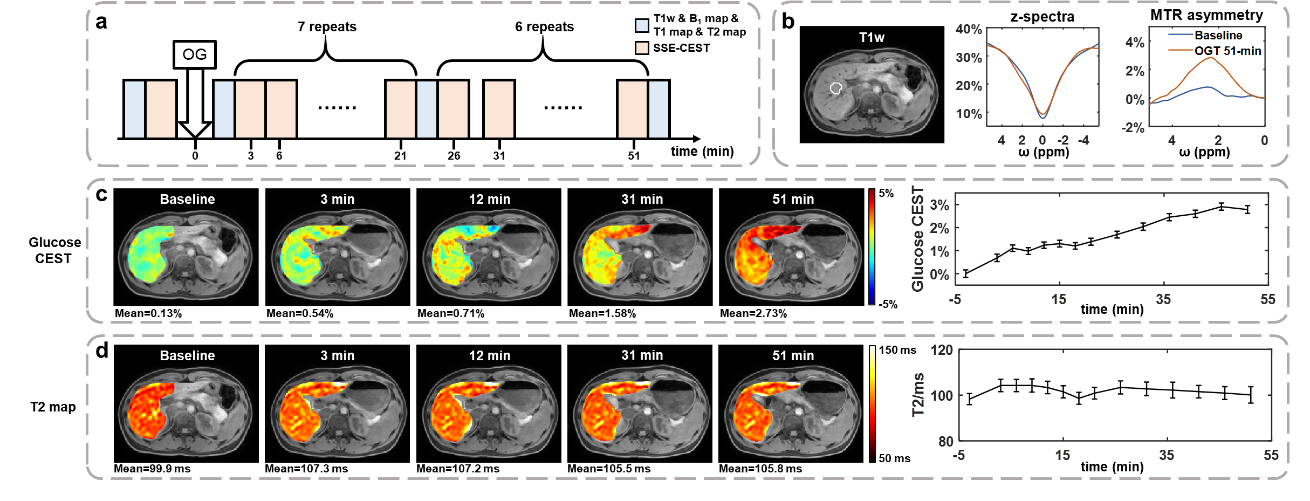
图5 SSE-CEST 技术在OGTT实验中用于动态葡萄糖成像
4、肝癌活性病灶与坏死鉴别
在HCC患者中,活性病灶在0.7 μT的LD图上呈现显著高信号(酰胺CEST、脂肪族NOE、糖原NOE均较坏死组织显著升高,p均<0.01);而坏死灶在所有对比中均为低信号(图6)。APTw(2 μT)未能显示显著差异,提示小B1多池LD分析更具特异性。SSE-CEST代谢图与FDG-PET/CT热区高度匹配,展现出“无标记、无辐射”监测治疗反应的潜力(图7)。
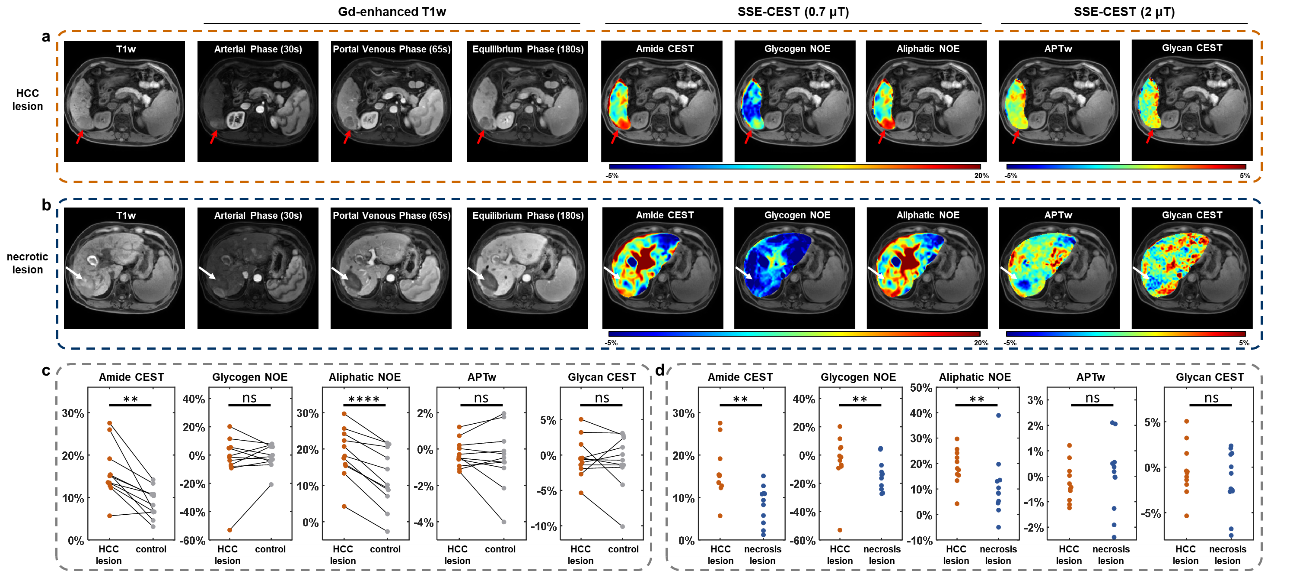
图6 SSE-CEST 技术对肝细胞癌病灶及坏死病灶的三维肝脏代谢图谱分析
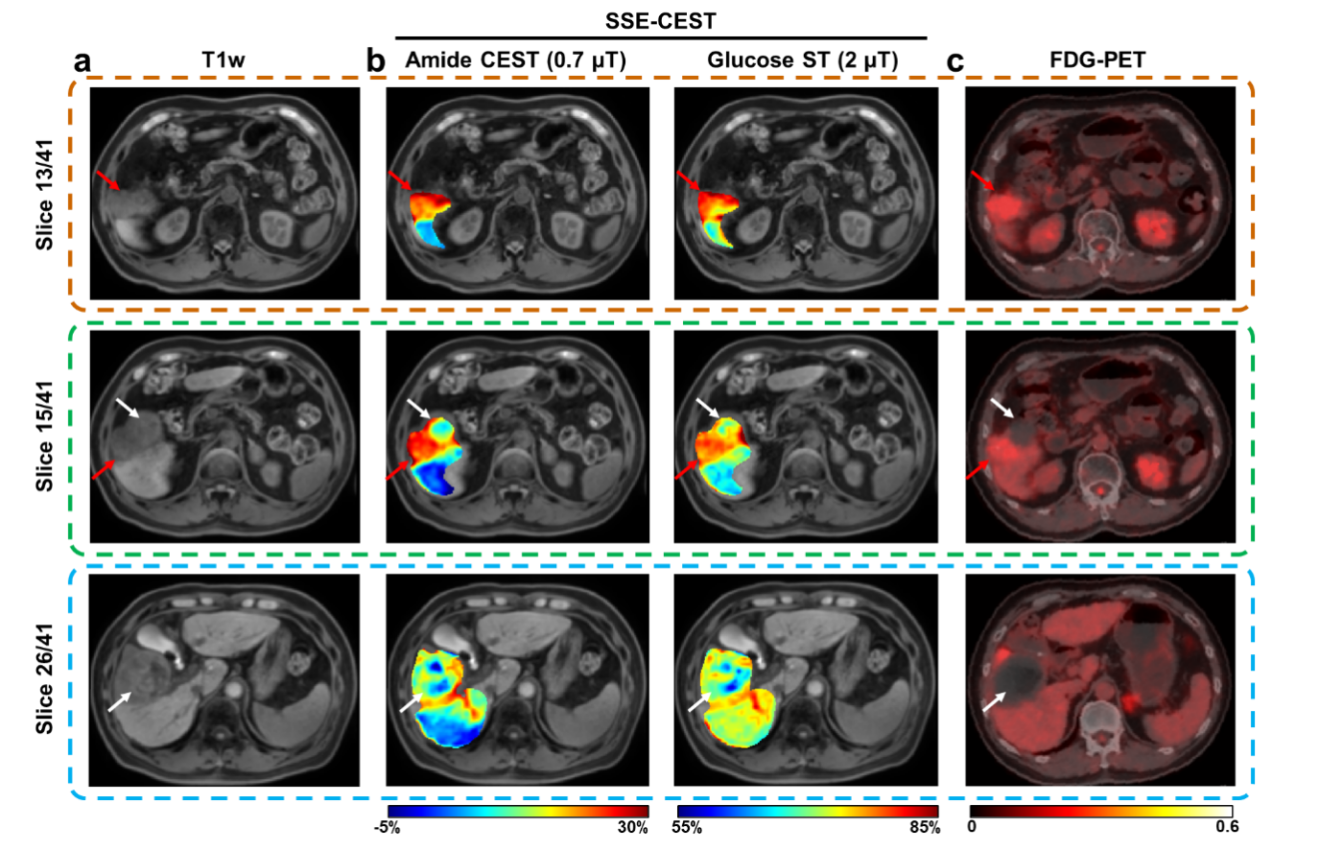
图7 一位HCC患者的 SSE-CEST 代谢图与 FDG-PET 图像的对比,该患者在治疗后 10 个月进行扫描
研究结论
本研究首次实现了单次屏气、3D全肝覆盖、无外源性标记的CEST代谢MRI,成功克服了腹部CEST长期存在的呼吸运动敏感与扫描时间过长两大临床障碍。SSE-CEST可同时探测多种内源性代谢物,在肝癌活性病灶与治疗后坏死的鉴别中表现优异,并与PET/CT结果高度一致。该技术有望成为肝脏及腹部疾病无创代谢成像的新范式。
清华大学生物医学工程学院2022级博士生刘础雨为论文第一作者、2023级高楠为论文共同第一作者,清华大学生物医学工程学院宋小磊副教授为论文通讯作者。
原文链接:https://www.nature.com/articles/s41467-026-71124-5