科学背景:
深麻醉下的大脑,真的只是“开”和“关”吗?
━━━━
在深麻醉、昏迷、低温以及部分病理性无意识状态中,大脑常常会出现一种非常典型的活动模式,称为爆发-抑制节律(burst-suppression)。从宏观脑电图上看,这种节律非常像一个周期性“开关”: 一段时间内,大脑出现高幅度的电活动爆发,随后又进入近乎平坦的低活动抑制状态。也正因为这种宏观波形十分醒目,长期以来,爆发-抑制常被理解为全皮层在“整体开启”(on state)和“整体沉默”(off state)之间来回切换。
但问题是:脑电信号中的“平坦”,真的意味着神经元都停止活动了吗?爆发出现时,是否真的代表整个皮层同时被激活?从抑制到爆发的转换,是全脑同步发生,还是具有更精细的时空组织?这些问题之所以长期难以回答,核心在于一个“跨尺度观测”难题。宏观脑电和皮层脑电图(ECoG)能够以毫秒级速度捕捉电活动变化,却难以看清具体是哪一批神经元参与其中;单细胞钙成像能够解析神经元活动,但往往难以同时覆盖足够大的皮层范围,并与高速电生理信号严格对齐。
要真正理解爆发-抑制节律,需要把两件事放到同一张“时间-空间地图”上:一边是宏观电信号,另一边是万级单神经元活动。
技术突破:
把全皮层单细胞成像和毫秒级电生理放到同一时间轴
━━━━
针对这一跨尺度观测瓶颈,清华大学戴小川、戴琼海、吴嘉敏课题组合作构建了皮层尺度光电融合观测系统CODE(Cortex-wide Optical-electrical Dual-modal Explorer)。该系统基于戴琼海院士团队此前研发的 RUSH 超大视场高分辨成像平台[1],并集成透明多通道ECoG电极阵列。简单来说,研究团队将传统颅窗变成了一个透明的“光电窗口”:既可以让显微镜看清皮层中的神经元,也可以同步记录皮层表面的电生理信号。相关研究成果以“Dynamic neuronal ensembles encode burst-suppression revealed by cortex-wide optical-electrical interfaces”(全皮层光-电双模态神经接口揭示爆发-抑制节律由动态神经元集群编码)为题,发表于《自然·通讯》(Nature Communications)。

点击查看更多论文信息
在实验中,研究团队能够在小鼠背侧皮层范围内同步记录约1.8万个神经元的钙活动,并将其与多个皮层区域的 ECoG 信号进行时间对齐。这为解析爆发-抑制节律中的跨尺度神经活动组织提供了关键基础。
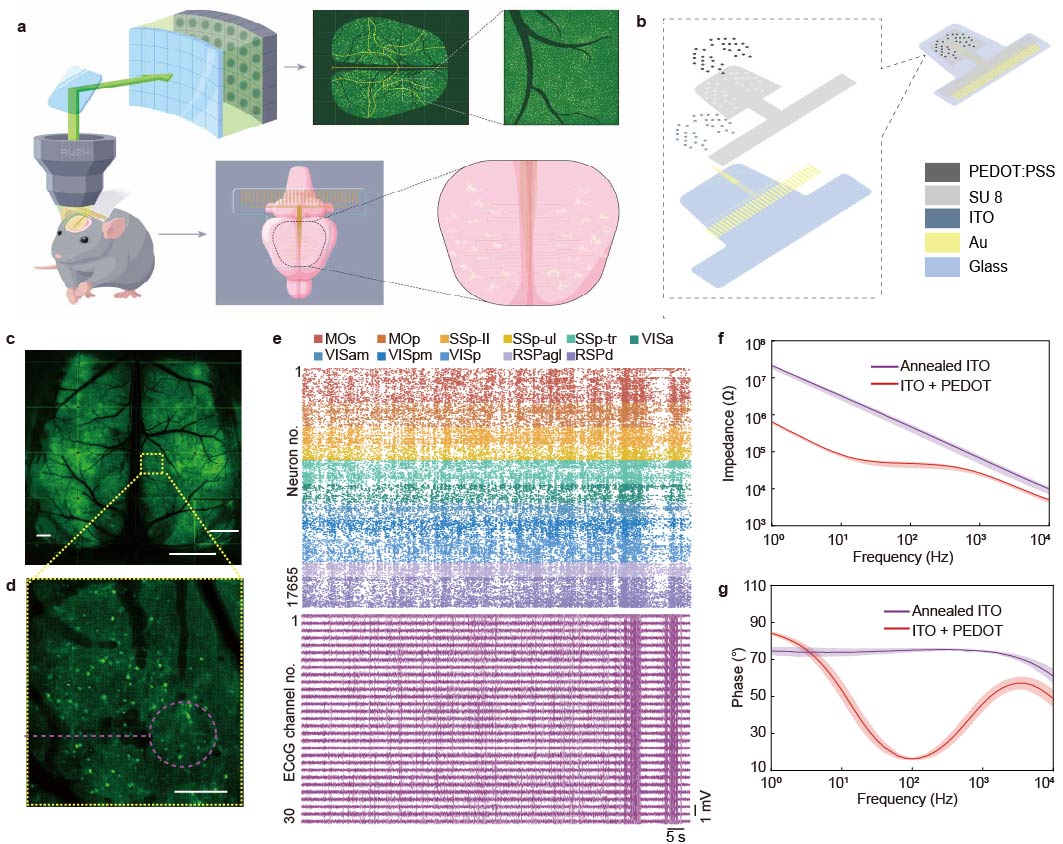
图1:全皮层光电融合记录系统 CODE
CODE系统将透明ECoG阵列与超大视场单细胞钙成像平台相结合,可在小鼠背侧皮层范围内同步获取大规模神经元活动和多区域电生理信号,为解析爆发-抑制节律中的跨尺度神经组织提供观测基础。
核心发现一:
深麻醉下的大脑,并不是整片皮层一起“开关”
━━━━
基于CODE系统,研究团队在异氟烷麻醉小鼠中同步记录全皮层ECoG信号和万级神经元钙活动。随着麻醉加深,ECoG信号中出现典型的爆发-抑制节律:高幅爆发与低活动抑制交替出现。与此同时,神经元钙活动也呈现出明显的状态依赖变化。
进一步分析神经元活动模式后,研究团队识别出两类神经元群体:一类在爆发期更活跃;另一类在抑制期更活跃。这意味着,ECoG信号中的“抑制”并不等同于皮层神经元完全沉默。在宏观看似平坦的阶段,仍然存在一类更分散、更异步的神经元活动。换句话说,爆发与抑制并不是同一批神经元活动强弱的简单变化,而是不同神经元群体在不同状态下呈现出的交替组织方式。
这也改变了我们对爆发-抑制节律的直观理解:深麻醉下的大脑并不是整片皮层同时“打开”或“关闭”,而是存在更精细的神经群体分工和动态接替。
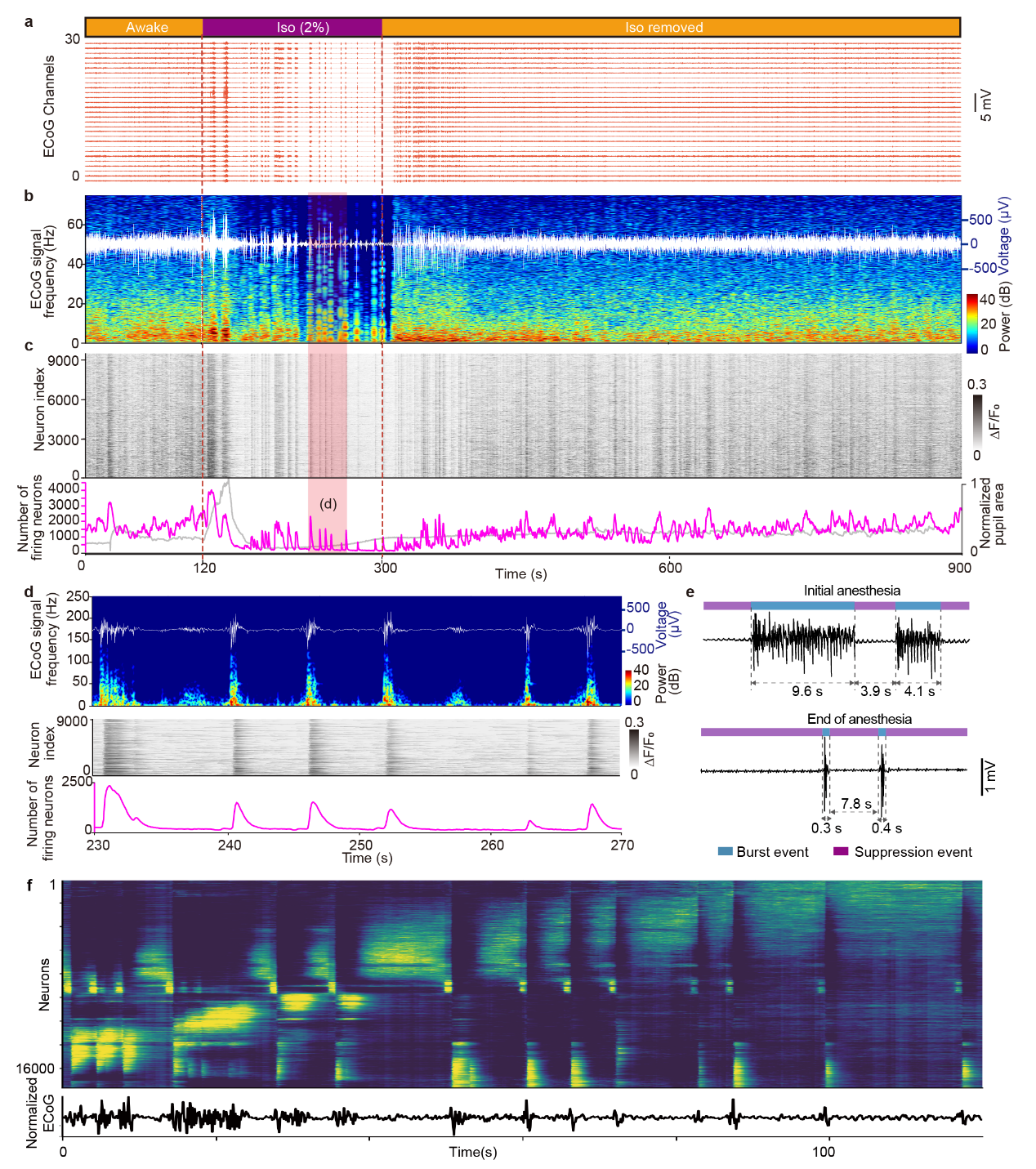
图2:爆发-抑制状态下两类神经元群体交替激活
研究识别出爆发相关神经元和抑制相关神经元两类活动群体。二者分别在爆发期和抑制期更活跃,并随爆发-抑制节律交替出现,说明该脑状态并非简单的整体同步开关,而具有明确的神经群体组织结构。
核心发现二:
爆发和抑制,不是固定模板的重复播放
━━━━
研究团队进一步追踪这两类神经元群体在整个麻醉过程中的变化。结果发现,爆发相关神经元和抑制相关神经元并不是固定不变的两群神经元。
随着麻醉进程推进,爆发事件持续时间逐渐缩短,参与爆发的活跃神经元数量也随之减少;抑制期逐渐延长,但参与抑制相关活动的神经元数量也呈减少趋势。跨事件追踪显示,每一次爆发或抑制事件中,既包含新参与的神经元,也包含此前曾经参与过的神经元。近期被招募的神经元更容易在后续事件中再次出现。这说明,爆发-抑制节律不是固定神经元模板的机械重复,而是一个持续变化的神经群体重组过程。
在时间结构上,爆发相关神经元通常在爆发早期快速达到活动峰值,表现出更强的同步性;抑制相关神经元则在抑制阶段较晚出现活动峰,整体活动更加分散。功能连接分析也显示,爆发期神经元之间的相关性和网络连接强度更高,而抑制期神经元活动更弱、更分散。这种差异有助于解释为什么宏观 ECoG中爆发期表现为高幅波形,而抑制期表现为低幅或近乎平坦的信号。
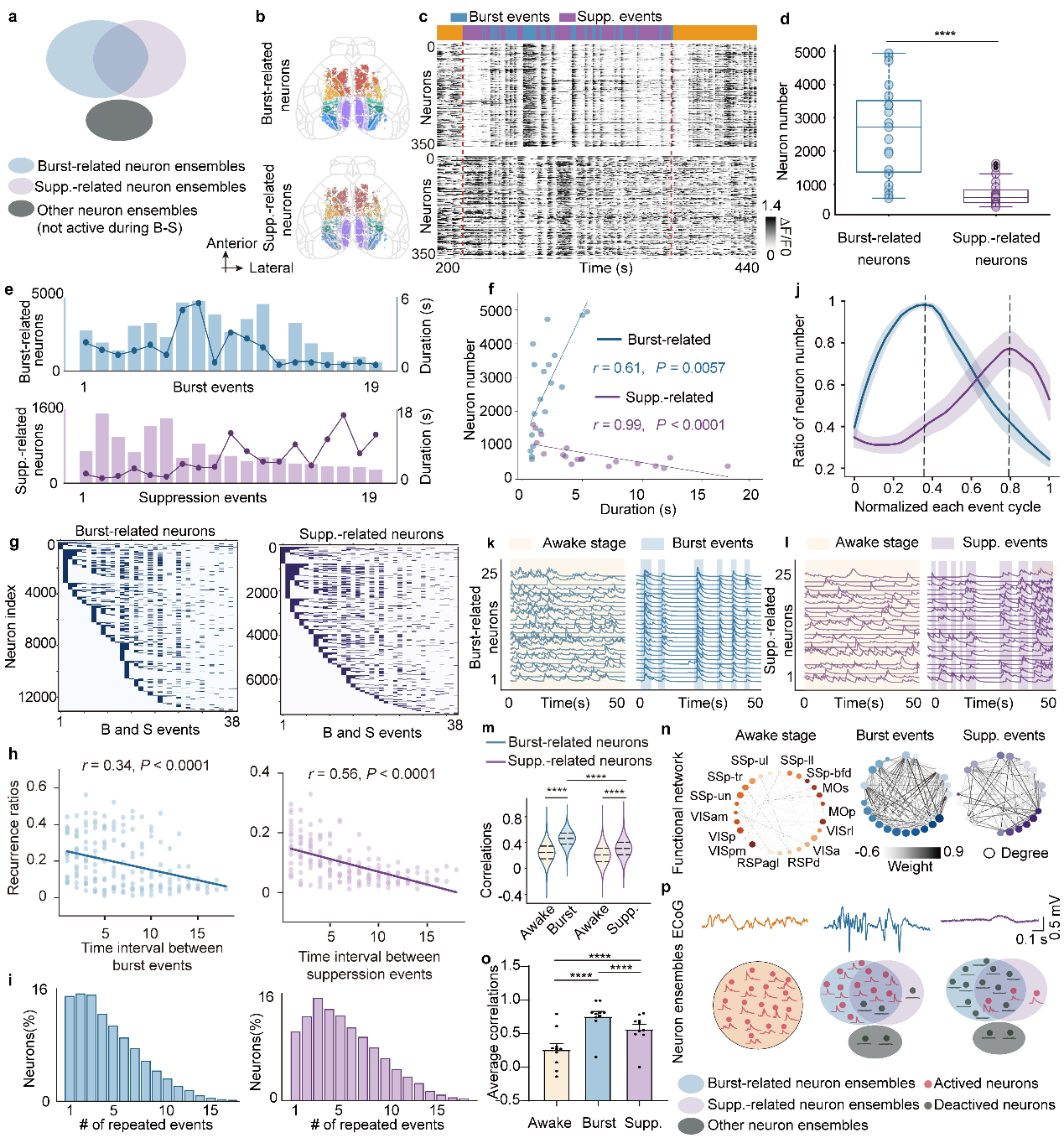
图3:爆发-抑制状态下神经元群体的动态招募与功能连接
爆发相关神经元在爆发早期快速同步激活,并形成更强的功能连接;抑制相关神经元则更晚、更分散地被招募,连接强度较弱。两类神经群体的不同组织方式共同塑造了宏观ECoG中爆发与抑制的波形差异。
核心发现三:
状态转换具有时空结构,而不是瞬间全局切换
━━━━
如果爆发-抑制不是简单的整体开关,那么从抑制到爆发的转换过程本身,也可能具有可观测的时空结构。
研究团队进一步分析了抑制向爆发转换过程中的皮层活动变化。通过对多通道ECoG信号进行空间分组和时间对齐分析,研究发现,爆发出现前后,不同皮层区域的电活动并非完全同时变化,而是沿着稳定的空间路径传播:爆发活动通常首先出现在双侧外侧感觉皮层,随后向内侧及前方运动相关区域推进。
单细胞钙活动与这一电生理传播过程高度对应。外侧感觉皮层附近的神经元活动峰较宽、时间分布更分散,而内侧运动相关区域的神经元活动峰更加尖锐,并与爆发起始时间更紧密对齐。光电跨模态互相关分析显示,ECoG与钙活动之间的同步性在传播过程中逐步增强,呈现出“边传播边同步”的特征。
这一发现进一步打破了爆发-抑制作为“全局同步事件”的简单认识。爆发并不是一开始就同时覆盖整个皮层,而是在从感觉相关区域向运动相关区域传播的过程中,逐步形成更强的神经元同步和跨模态耦合。也就是说,即便在深麻醉状态下,皮层活动仍然不是完全随机或均一的,而是保留了可解析的时空组织特征。
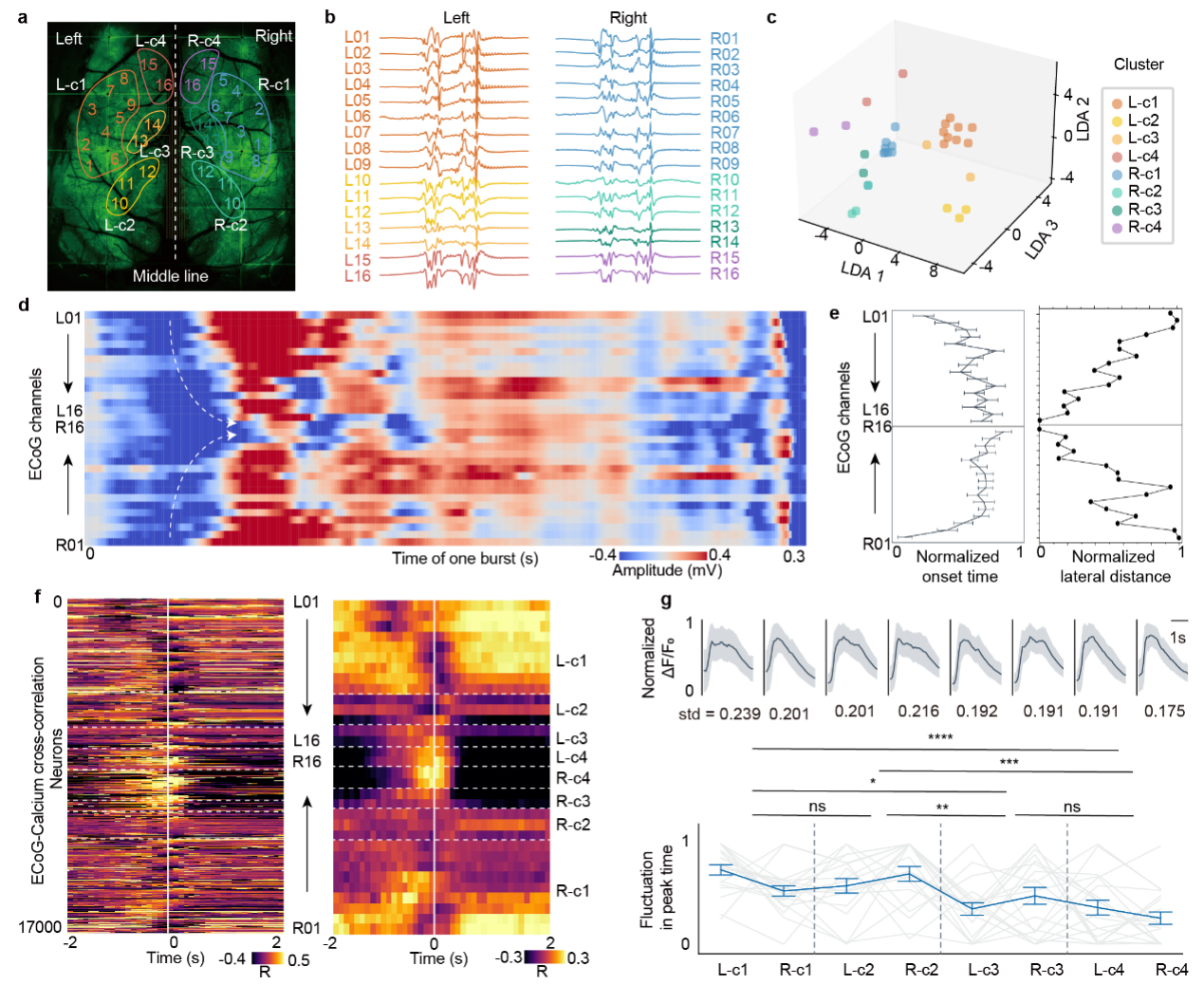
图4:抑制向爆发转换过程中,皮层活动的有序传播
多通道ECoG与单细胞钙成像共同显示,抑制向爆发转换过程中,皮层活动并非全局同步出现,而是呈现出区域间的时序差异和动态组织结构,提示深麻醉状态下的皮层转换仍具有可解析的时空特征。
跨模态解析:
宏观脑电何时能够“读懂”单细胞活动
━━━━
在揭示爆发-抑制中的神经群体组织和时空动态后,研究团队进一步提出了一个问题:宏观ECoG信号在多大程度上能够反映底层单细胞神经元活动?
为回答这个问题,研究团队建立了跨模态预测框架。首先,从多通道ECoG信号中提取时域和频域特征;同时,利用共享方差成分分析(shared variance component analysis, SVCA)对万级神经元钙活动进行低维表征;随后,通过reduced-rank regression建立ECoG特征到钙信号共享方差成分的预测模型,并进一步重建神经元群体活动。
结果显示,ECoG对钙活动的预测能力具有明显的脑状态依赖性:在清醒状态下预测效果最低,在抑制期有所提高,在爆发期最高。
这说明,宏观脑电信号并不是在所有状态下都以同样方式反映精细的神经元活动。当神经元活动更加同步、网络耦合更强、群体动力学更低维时,ECoG更容易捕捉到其对应的群体活动结构;而在清醒状态下,神经活动更加复杂和高维,宏观电信号与单细胞活动之间的对应关系也相对减弱。
这一结果为理解宏观脑电信号的可解释性提供了定量视角:我们不能简单地把ECoG或EEG看作神经元活动的直接“平均值”,它们在不同脑状态下所反映的精细神经活动结构与程度可能并不相同。
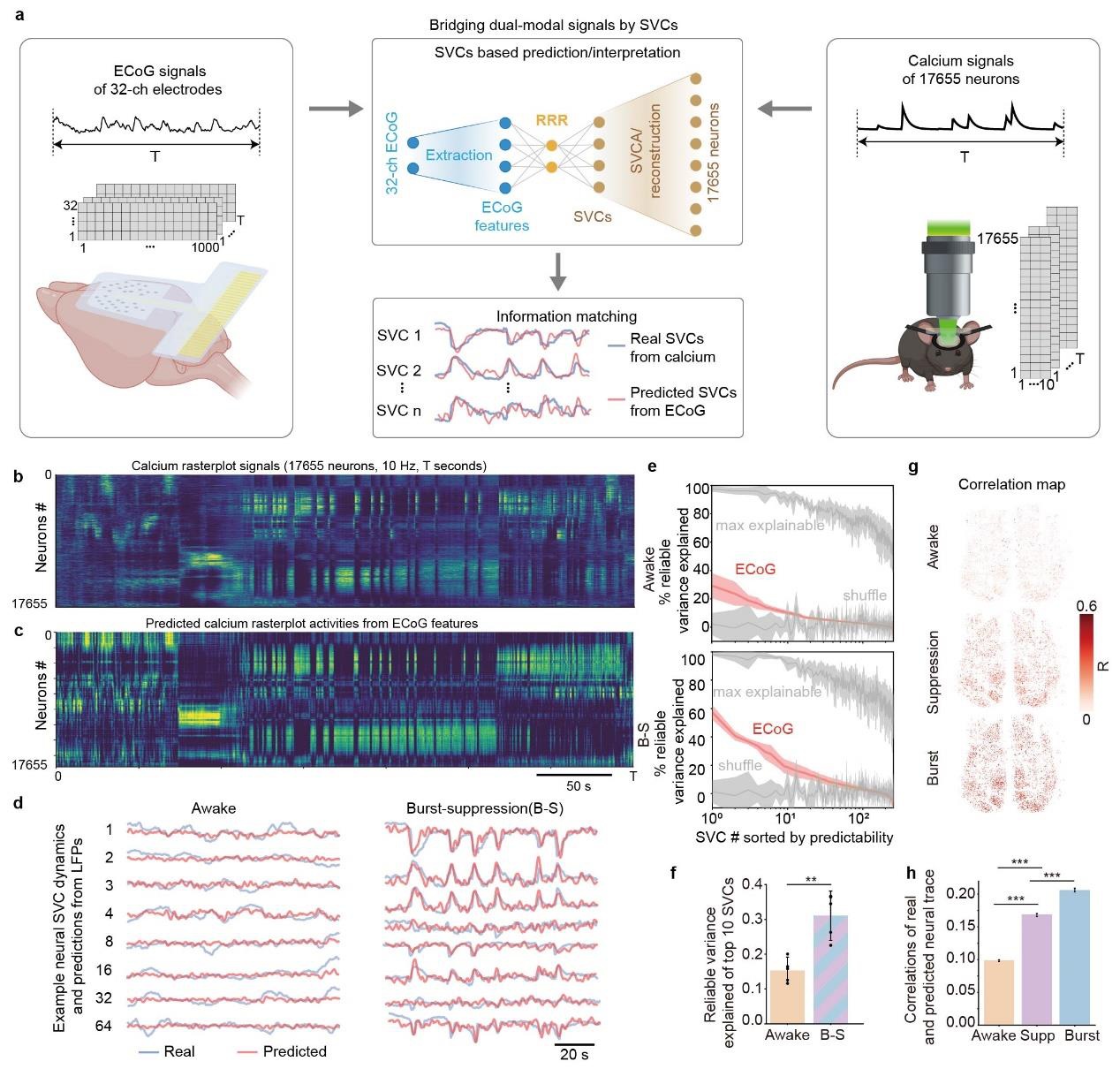
图5:基于共享方差成分的光电双模态信号关联与跨模态预测
研究通过共享方差成分和跨模态预测模型,将宏观ECoG特征与万级神经元钙活动联系起来。结果表明,ECoG对钙活动的预测能力具有明显脑状态依赖性,在爆发期最高、抑制期次之、清醒状态最低。
总结与展望
爆发-抑制是一种有组织的皮层动态状态
━━━━
本研究通过CODE系统,将万级单神经元钙成像与多区域ECoG电生理记录放到同一时间轴上,系统解析了深麻醉下爆发-抑制节律的跨尺度组织规律。
研究发现:
第一,爆发和抑制并非同一神经群体活动强弱的简单交替,而是由不同神经元群体在不同阶段呈现出偏好性活动。
第二,爆发期表现为更强同步性和更高功能连接,而抑制期则呈现更分散、更异步的活动。
第三,抑制向爆发的转换过程具有可解析的皮层时空结构,而不是简单的全局同步切换。
第四,宏观ECoG信号对底层单细胞群体活动的解释能力依赖于脑状态,在高度同步的爆发期最强,在复杂高维的清醒状态下相对减弱。
这些发现表明,爆发-抑制并不是一个均一、被动的全皮层静默过程,而是一种由神经群体动态招募、功能连接变化和跨区域时空组织共同塑造的复杂脑状态。
展望未来
CODE所展示的光电融合观测能力,为未来研究提供了新的工具和思路
━━━━
• 解析脑状态转换的跨尺度规律:通过同时捕捉高速电生理节律和微观神经元群体活动,CODE有望用于进一步研究麻醉、睡眠、昏迷、癫痫等不同脑状态下的动态转换过程。
• 发展可解释的脑状态监测方法:通过建立ECoG与单细胞群体活动之间的跨模态对应关系,该研究为理解宏观脑电信号在不同意识状态下的神经基础提供了新的量化框架。
• 拓展至细胞类型、神经调质和疾病模型研究:未来结合更高密度透明电极阵列、更宽带电生理记录技术以及细胞类型特异成像方法,有望进一步提高对皮层动力学的解析精度,并拓展至复杂认知任务和神经疾病模型研究。
清华大学信息国家研究中心副研究员肖桂花、生物医学工程学院2020级博士生杨默、自动化系博士后李灵博为该文章共同第一作者。清华大学生物医学工程学院戴小川副教授、自动化系戴琼海院士、自动化系吴嘉敏副教授、信息国家研究中心肖桂花副研究员为该论文共同通讯作者。合作者还包括清华大学生物医学工程学院洪波课题组及北京大学材料科学与工程学院雷霆课题组。 |
原文链接:https://www.nature.com/articles/s41467-026-72454-0
参考文献:[1] Fan, J. T. et al. Video-rate imaging of biological dynamics at centimetre scale and micrometre resolution. Nature Photonics 13, 809 (2019). https://doi.org:10.1038/s41566-019-0474-7.